ADEGUATEZZA DEI METODI DI CONTROLLO GLICEMICO NEI DIABETICI
Enrico Bologna
Specialista in Medicina Interna, Gastroenterologia e Patologia generale.
Già Primario Ospedale Fatebenefratelli, Isola Tiberina, Roma.
Libero docente in Patologia Medica, Università di Roma “Sapienza”.
Riassunto.
Il concetto di adeguatezza del controllo glicemico è stato recentemente sottoposto a revisione, in base alle osservazioni relative alla responsabilità delle oscillazioni glicemiche nelle complicazioni del diabete. Vengono qui discussi i metodi utilizzabili per il controllo della glicemia, con particolare attenzione per i marker non tradizionali di iperglicemia.
Summary. Adequacy of current methods for glycemic control
In diabetic patientsThe concept of adequacy of blood glucose control has evolved in last years according the observations of the correlation between glucose variability and diabetes complications. In this paper the various blood glucose monitoring methods are reviewed, focusing on the nontraditional markers of hyperglycemia.
___________________________
L’esistenza di un rapporto diretto tra qualità del controllo glicemico e rischio di complicazioni micro- e macrovascolari del diabete mellito è stata dimostrata da numerose ricerche, in particolare dal Diabetes Control and Complications Trial (DCCT) e dal United Kingdom Prospective Diabetes Study (UKPDS) 24,25. Ma il concetto di adeguatezza del controllo glicemico è andato modificandosi nel tempo, in rapporto con i metodi di utilizzati. Metodi che, a partire dalla ricerca della glicosuria, sono giunti oggi al monitoraggio glicemico continuo, premessa alla creazione del “pancreas artificiale”. Nell’ambito del controllo glicemico, da alcuni anni è oggetto di ampia discussione l’importanza della variabilità glicemica, definita come l’insieme degli episodi circadiani di ipo- e iperglicemie, soprattutto postprandiali. Alla frequenza ed entità di questi episodi viene infatti attribuita grande responsabilità nelle complicazioni del diabete. I picchi iperglicemici, in particolare, più ancora della iperglicemia persistente inducono una aumentata produzione di radicali liberi e di vari mediatori dell’infiammazione provocando disfunzione endoteliale e delle β-cellule pancreatiche 1,4. I picchi glicemici assumono perciò grande rilevanza non solo nella patogenesi delle complicazioni del diabete ma anche nell’esaurimento della produzione di insulina. Il danno si realizza quando l’eccesso glicemico determina la glicosilazione non enzimatica di aminoacidi liberi ovvero di proteine presenti nel sangue o nei tessuti; questo fenomeno, inizialmente reversibile, diviene poi irreversibile attraverso una serie di reazioni (Fig. 1). I prodotti finali glicosilati (Advanced Glycosilation End products (AGEs) si accumulano nei tessuti legandosi al collageno. Inoltre l’interazione tra AGEs e specifici recettori (RAGE) genera specie reattive dell’ossigeno (Reactive Oxygen species, ROS). Se i livelli dei ROS superano le capacità difensive rappresentate dall’intervento di vari enzimi (superossidodismutasi, catalasi, lactoperossidasi, glutatione perossidasi e perossiredoxine), oltre che da acido ascorbico, tocoferolo e acido urico, si realizzano una serie di azioni lesive comprendenti danno del DNA, perossidazione lipidica e proteica, inattivazione di enzimi3,20,21. Non meno importanti in rapporto alle complicazioni cardiovascolari, anche se molto meno considerate, sono le ipoglicemie la cui azione dannosa, in buona parte mediata da brusche e intense attivazioni del sistema simpatico, è stata recentemente dimostrata da una metanalisi relativa ad oltre 900.000 soggetti con diabete mellito tipo 2: nei pazienti in cui sono state registrate le più gravi ipoglicemie il rischio di malattia cardiovascolare è apparso più che raddoppiato 10.
Nella attuale pratica clinica la valutazione del controllo glicemico viene effettuata, oltre che mediante le automisurazioni ripetute nella giornata con l’uso dei glucometri, soprattutto con la determinazione dell’ emoglobina glicata (HbA1c). Quando i globuli rossi entrano in circolo contengono quantità minime di glucosio; essendo però dotati di una membrana liberamente permeabile al glucosio, questo vi penetra e si lega irreversibilmente all’emoglobina in misura direttamente dipendente dalla concentrazione glicemica prevalente. Poiché ogni 24 ore circa l’1% degli eritrociti vengono distrutti ed una quota equivalente viene immessa in circolo, il livello di HbA1c rappresenta una misura dinamica della glicemia media esistente durante la permanenza in circolo degli eritrociti. La correlazione con la glicemia media è massima per le 8-12 settimane precedenti il prelievo. La validità della HbA1c può trovare dei limiti nella ancora non generalizzata standardizzazione dei metodi di laboratorio e in tutte le condizioni che alterano la sopravvivenza degli eritrociti in circolo: valori falsamente elevati possono aversi quando il ricambio eritrocitario è rallentato, come avviene in presenza di deficit di ferro, vitamina B12 o folati. Al contrario, valori falsamente bassi di HbA1c si osservano quando il ricambio eritrocitario è accelerato, come in caso di emolisi o di anemie nonché in corso di trattamenti volti correggere stati anemici con l’uso di ferro, vitamina B12 o folati e nei pazienti che ricevono eritropoietina. Soggetti particolarmente esposti a falsi risultati sono quelli con insufficienza renale, specialmente se in trattamento con eritropoietina. Sono state osservate anche differenze razziali dei valori di HbA1c (più elevati in Ispanici, Asiatici e Afroamericani), ma tali differenze sono ben poco significative da un punto di vista pratico. Il limite principale della misurazione della HbA1c è rappresentato dalla incapacità dell’esame di fornire informazioni sulla variabilità circadiana della glicemia, in quanto valori uguali possono essere determinati da oscillazioni glicemiche di entità molto differenti.
Come accennato, il metodo attualmente più diffuso per valutare le oscillazioni glicemiche nel corso della giornata è rappresentato dall’autocontrollo della glicemia e si basa sull’uso dei glucometri, nei quali la misurazione è operata da un fotometro capace di misurare la reazione tra il glucosio presente nel sangue capillare e un enzima contenuto nella striscia reattiva, rappresentato da glucosio-ossidasi o glucosio-deidrogenasi. I metodi basati sull’uso del primo enzima sono specifici in quanto non sensibili ad altri glicidi, ma forniscono valori superiori alla realtà in situazioni di ipossia di origine fisiologica (altitudine) o patologica (insufficienza respiratoria)(19). I glucometri che utilizzano la glucosio-deidrogenasi non sono influenzati dalla concentrazione di ossigeno nel sangue ma per data la presenza di un cofattore necessario per la reazione (pirrolochinolina) sono sensibili ad altri glicidi come ad esenpio il maltosio, che nei soggetti in dialisi peritoneale deriva dalla icodestrina presente nel liquido di dialisi, con il risultato di sovrastima della glicemia 26.
Recentemente è stata condotta una approfondita ricerca sull’accuratezza dei risultati forniti da 34 glucometri utilizzati in Europa, valutati secondo i criteri dellostandard DIN EN ISO 15197:2003: i requisiti minimi sono stati raggiunti da 27 apparecchi (79,4%), ma solo 18 (52,9%) hanno soddisfatto i più restrittivi criteri richiesti da una recente revisione di ISO15197 7. Oltre ai problemi relativi ai singoli glucometri vanno tenute presenti le ben note cause di errore dipendenti dalla correttezza del prelievo e delle manualità necessarie per l’esecuzione del test.
Nel 2011 è stata pubblicata una raccomandazione redatta da esperti relativamente alle modalità di autocontrollo glicemico nei soggetti con diabete mellito tipo 2 22. Queste raccomandazioni prevedono un metodo non intensivo (un prelievo prima e due ore dopo un pasto, da tre a sette volte alla settimana per una settimana al mese) ed una intensiva, riservata ai soggetti con cattivo controllo metabolico e trattamento insulinico o con dosi multiple di ipoglicemizzanti orali (prelievi prima e due ore dopo tutti i pasti da tre giorni alla settimana a una settimana al mese). E’ del tutto evidente che, anche con una elevata frequenza di controlli, eventuali picchi e nadir glicemici che si verificano in altri momenti della giornata, in particolare notturni ovvero nei giorni in cui i prelievi non vengono eseguiti, sfuggono all’osservazione.
L’unico mezzo capace di fornire una conoscenza diretta e completa dell’andamento glicemico è rappresentata dai sistemi di misurazione continua della glicemia (Continuous Glucose Monitgoring System, CGMS). Due i principali tipi di CGMS: i Retrospective o Professional CGMS, che registrano le misurazioni effettuate ogni 5 minuti per 3-5 giorni (288 letture/die), misurazioni che possono poi essere visualizzate dal medico nel suo studio, e i real time CGMS. Questi sono dotati di un monitor che permette di seguire i valori glicemici momento per momento e possono inoltre essere collegati ad una pompa di insulina. Entrambi i tipi di apparecchi utilizzano un sensore sottocutaneo elettrochimico (glucosio ossidasi) che trasmette ad un monitor la corrente generata dalla ossidazione del glucosio. 8,9,11.
Le misurazioni fornite dai CGMS, che hanno dimostrato di consentire un miglior controllo metabolico soprattutto nel diabete mellito tipo 2, 14. possono differire da quelle condotte su sangue venoso. La concentrazione di glucosio nel liquido interstiziale in cui è posto il sensore, infatti, è minore rispetto a quella presente nel sangue venoso nelle fasi di rapida variazione glicemica; l’accuratezza è in genere buona con valori glicemici elevati (240-400 mg/dL) mentre lo è molto meno in condizioni di ipoglicemia (<70 mg/dL) 2,16.
I metodi di controllo continuo della glicemia, costosi e ancora in evoluzione, sono certamente inadatti a studi su ampio casistiche destinati a stabilire l’importanza della variabilità glicemica nei confronti delle complicazioni del diabete ed infatti sono stati utilizzati a tal fine solo su poche casistiche in genere relative a popolazioni limitate. Una ricerca condotta su 59 diabetici in trattamento con sola dieta o anche con ipoglicemizzanti orali ha preso in esame la correlazione tra ampiezza delle oscillazioni glicemiche registrate in monitoraggio continuo per 3 giorni consecutivi e funzione β-cellulare valutata mediante misurazioni della glicemia e del C-peptide in rapporto al pasto15. I risultati hanno dimostrato l’esistenza di una significativa correlazione non lineare tra variabilità glicemica e funzione pancreatica (Fig. 2) ma non con altri parametri quali l’apporto glicidico e la sensibilità all’insulina.
In una popolazione di soggetti con diabete mellito tipo 2 a confronto con soggetti non diabetici l’entità delle fluttuazioni glicemiche valutata mediante monitoraggio continuo è risultata inversamente correlata sia con il trofismo della materia grigia nel sistema limbico e nei lobi temporo-parietali, sia con la capacità cognitiva 5. In un altro studio l’ampiezza delle oscillazioni glicemiche, valutata con monitoraggio continuo in 216 soggetti con diabete mellito tipo 2, è apparsa associata al rilievo di placche arteriose carotidee e intracraniche così come allo spessore intima-media della carotide. In base a queste osservazioni gli autori concludono che la variabilità glicemica si comporta come un fattore contribuente all’aterosclerosi subclinica al pari di età e di pressione arteriosa sistolica 17.
La disponibilità di un esame come HbA1c, che fornisce informazioni sull’andamento glicemico nelle precedenti 8-12 settimane, rappresenta certamente uno strumento diagnostico di grande utilità, ma il suo impiego non deve indurre, come spesso avviene, a ridurre la frequenza della automisurazione mediante glucometro che rimane il mezzo più semplice anche se meno comodo per controllare le variazioni circadiane della glicemia.
Recentemente vi è stato un crescente interesse verso marker non tradizionali di iperglicemia quali fruttosamina, albumina glicata e 1,5-anhydroglucitolo (1,5-AG). Questo interesse è collegato a numerose recenti osservazioni secondo cui questi marker rappresentano buoni indicatori delle complicanze micro- e macrovascolari del diabete. Inoltre la misurazione della fruttosamina e dell’albumina glicata si è dimostrata in grado di migliorare l’identificazione dei soggetti diabetici.
Per quanto riguarda in particolare la valutazione della variabilità glicemica, qualche vantaggio può derivare dalla misurazione della fruttosamina. E’ questa una ketoamina che si forma per effetto della glicosilazione e che è caratterizzata da un ricambio molto più rapido rispetto ad HbA1c; per tale motivo essa riflette la glicemia media delle ultime 1-2 settimane. I metodi di misura sono più economici e più rapidi rispetto a quelli necessari per determinare HbA1c; a questo vantaggio fanno riscontro una maggiore variabilità intraindividuale e la necessità di correggere il risultato secondo la concentrazione plasmatica di albumina soprattutto in casi di rapido turnover di questa proteina (enteropatie proteino-disperdenti, sindrome nefrosica 12,13.
Una valutazione dell’andamento glicemico nelle 24 ore precedenti può essere invece ottenuta dalla misurazione di 1,5-AG,che inoltre sembra particolarmente sensibile alle iperglicemie postprandiali Si tratta di un poliolo di origine alimentare che in condizioni normali viene filtrato dai glomeruli renali e completamente riassorbito nei tubuli. Poiché il riassorbimento è inibito competitivamente dal glucosio, quando la glicemia supera la capacità dei tubuli di riassorbire il glucosio filtrato, l’aumento del glucosio nel liquido tubulare ostacola il riassorbimento di 1,5-AG, la cui concentrazione plasmatica perciò si riduce in misura proporzionale all’iperglicemia 6.
Così la misurazione di \,5-AG riflette I valori glicemici delle ultime 24 ore, mentre quella di fruttosamina e di HbA1c indicano I valori glicemici medi delle ultime una-due settimane e rispettivamente degli ultimi due-tre mesi.
In una recente ricerca, condotta su oltre 10.000 soggetti, è stato osservato che nei diabetici bassi valori di 1,5-AG (< 6 µg/mL) sono risultati significativamente correlati con la presenza di retinopatia e con il rischio di nefropatia. Per contro, valori ≥ 10 µg/mL sono risultati correlati con la più bassa prevalenza di retinopatia e di rischio di nefropatia 23.
Secondo vari autori un più ampio uso dei marker non tradizionali di iperglicemia, se giustificato da ulteriori conferme cliniche, può permettere di superare i limiti di HbA1c in alcuni soggetti fornendo informazioni aggiuntive sul controllo glicemico a breve termine e migliorando la valutazione del rischio di complicazioni 18.
Fino a quando queste conferme non saranno state ottenute l’automisurazione ripetuta della glicemia rimarrà un elemento fondamentale, insieme al periodico controllo di HbA1c, per garantire una adeguata sorveglianza del trattamento ipoglicemizzante.
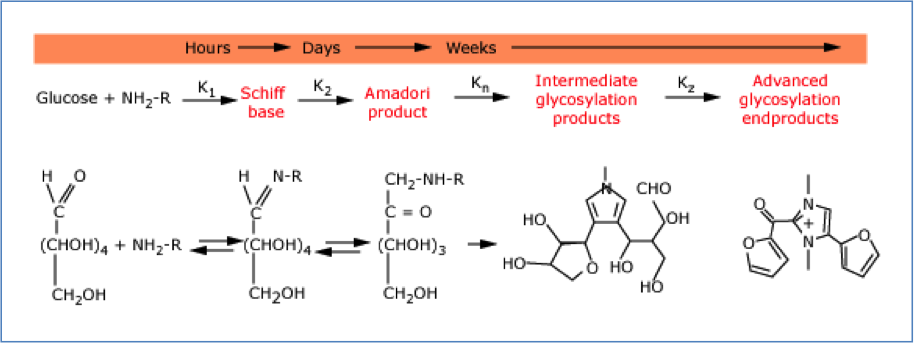
Fig. 1 (Modificata da 1)
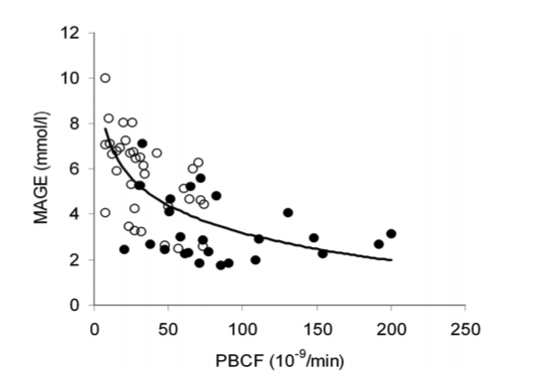
Rapporto tra ampiezza media delle oscillazioni glicemiche (Mean Amplitude of Glycemic Excursions, MAGE) e funzione beta-cellulare postprandiale (Postprandial Beta Cell Function, BCF) in diabetici trattati con sola dieta (◌) o anche con ipoglicemizzanti orali (●).
Fig. 2 (Da 15)
BIBLIOGRAFIA
1 BUCALA R, VLASSARA H, CERAMI A: Advanced glycosylated endproducts: role in diabetic and nondiabetic vascular disease. Drug Develop Res 1994:32,77.
2 CASTLE JR, PITTS A, HANAVAN K & al: The accuracy benefit of multiple amperometric glucose sensors in people with type 1 diabetes. Diabetes Care. 2012;35(4):706
3 CAVALOT F, PETRELLI A, TRAVERSA M & al: Postprandial blood glucose is a stronger predictor of cardiovascular events than fasting glucose in type 2 diabetes mellitus, particularly in women: lessons from the San Luigi Gonzaga Study. J Clin Endocrinol Metab 2006:91,813
4 CERIELLO A : Postprandial hyperglycemia and diabetes complications: is it time to treat? Diabetes 2005:54,1
5 CUI X, ABDULJALIL A, MANOR BD& al: Multi-scale glycemic variability: a link to gray matter atrophy and cognitive decline in type 2 diabetes. PLoS One. 2014:9,e86284.
6 DUNGAN KM, BUSE JB, LARGAY J & al: 1,5-anhydroglucitol and postprandial hyperglycemia as measured by continuous glucose monitoring system in moderately controlled patients with diabetes. Diabetes Care. 2006:29,1214
7 FRECKMANN G, SCHMID C, BAUMSTARK A & al:,Monitoring Systems for Self-Monitoring of Blood Glucose according to DIN EN ISO 15197. J Diabetes Sci Technol 2012:6,1060
8 GARG S, ZISSER H, SCHWARTZ S & al: Improvement in glycemic excursions with a transcutaneous, real-time continuous glucose sensor: a randomized controlled trial. Diabetes Care. 2006:29,44
9 GARG SK, SMITH J, BEATSON C & al: Comparison of accuracy and safety of the SEVEN and the Navigator continuous glucose monitoring systems. Diabetes Technol Ther. 2009:11,65
10 GOTO A, ARAH OA, GOTO M& al: Severe hypoglycaemia and cardiovascular disease: systematic review and meta-analysis with bias analysis. BMJ. 2013 Jul 29:347,f4533
11 HIRSCH IB: Clinical review: Realistic expectations and practical use of continuous glucose monitoring for the endocrinologist. J Clin Endocrinol Metab. 2009:94,223
12 HOWEY JE, BENNET WM, BROWNING MC & al: Clinical utility of assays of glycosylated haemoglobin and serum fructosamine compared: use of data on biological variation Diabet Med. 1989:6,793
13 HOWEY JE, BROWNING MC, FRASER CG: Assay of serum fructosamine that minimizes standardization and matrix problems: use to assess components of biological variation. Clin Chem. 1987:33,269
14 JUVENILE DIABETES RESEARCH FOUNDATION CONTINUOUS GLUCOSE MONITORING STUDY GROUP. N Engl J Med. 2008:359,1464
15 KOHNERT KD, VOGT L, AUGSTEIN P & al: Relationships between glucose variability and conventional measures of glycemic control in continuously monitored patients with type 2 diabetes.Horm Metab Res. 2009:41,137
16 MASTROTOTARO J, SHIN J, MARCUS A, SULUR G, STAR 1 Clinical Trial Investigators: The accuracy and efficacy of real-time continuous glucose monitoring sensor in patients with type 1 diabetes.Diabetes Technol Ther. 2008:10,385
17 MO Y, ZHOU J, LI M, WANG Y& al: Glycemic variability is associated with subclinical atherosclerosis in Chinese type 2 diabetic patients. Cardiovasc Diabetol. 2013 Jan 15;12:15. doi: 10.1186/1475-2840-12-15.
18 PARRINELLO CM, SELVIN E: Beyond HbA1c and glucose: the role of nontraditional glycemic markers in diabetes diagnosis, prognosis, and management. Curr Diab Rep. 2014:14,548
19 REBEL A, RICE MA, FAHY BG: Accuracy of point of-care glucose measurements. Diabetes Sci Technol 2012:6396
20 ROBERTSON RP : Chronic oxidative stress as a central mechanism for glucose toxicity in pancreatic islet beta cells in diabetes. J Biol Chem 2004:279,42351
21 SHIRAIWA T, KANETO H, MIYATSUKA T & al: : Postprandial hyperglycemia is a better predictor of the progression of diabetic retinopathy than HbA1c in Japanese type 2 diabetic patients. Diabetes Care 2005:28,2806
22 SCHNELL O, ALAWI H, BATTELINO T & al: Addressing schemes of self-monitoring of blood glucose in type 2 diabetes: A European perspective and expert recommendation. Diabetes Technol Ther 2011:13,959
23 SELVIN E, RAWLINGS AM2, GRAMS M& al: Association of 1,5-anhydroglucitol with diabetes and microvascular conditions. Clin Chem. 2014:60,1409
24 THE DIABETES CONTROL AND COMPLICATIONS TRIAL (DCCT) RESEARCH GROUP. The Effect of Intensive Treatment of Diabetes on the Development and Progression of Long-Term Complications in Insulin-Dependent Diabetes Mellitus. N Engl J Med 1993; 329:977-986
25 UK Prospective Diabetes Study (UKPDS) Group: Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33).. Lancet. 1998:352(9131):837-53.
26 U S FOOD AND DRUG ADMINISTRATION. FDA public health notification. Potentially fatal error with GDH-POQ glucose monitoring technology. August 13, 2009
