NOTIZIARIO Febbraio 2013 N°2
COMPLESSITÀ DELL’OBESITÀ
Obesità e cancro
A cura di:
Giuseppe Di Lascio §
Susanna Di Lascio***
Con la collaborazione di:
Il World Cancer Day 2013
Il cancro, com’è ormai noto, è una delle principali cause di morte nel mondo con i 7,6 milioni di decessi stimati nel 2008, pari a circa il 13% dei totali. Per questo ogni 4 febbraio di ogni anno la WHO sostiene l’International Union Against Cancer per promuovere i modi per alleviare il carico globale derivante da esso. In questa giornata, ripetutasi anche nel 2013, si discutono i temi ricorrenti di prevenzione e le strategie e le formule per accrescere la qualità della vita dei malati. Confortante è il rilievo, derivato dalle moderne tecnologie, capaci di rilevare nelle persone esposte la relazione tra le sempre nuove sostanze chimiche e la malattia. In tal modo gli scienziati stanno trovando di continuo sostegno nella definizione di un quadro completo sull’influenza degli inquinamenti dell'ambiente sulla salute.
In occasione della giornata mondiale contro il cancro di quest’anno, L’UICC (Union for International Cancer Control) si è proposta di contrastare i miti consolidatisi sulla malattia nel corso degli anni per cui è stata dipinta come una condanna a morte, come un appannaggio dei ricchi, come una patologia degli anziani e dei paesi sviluppati. In effetti, l’epidemiologia riporta ormai che più della metà delle morti per cancro, pari al 55%, ricorre nelle regioni meno sviluppate del mondo. Le previsioni, peraltro, entro il 2030 indicano circa il 60% - 70% di tutti i nuovi casi di cancro in questi paesi. Anche l’OMS (Organizzazione Mondiale della Sanità) afferma che due terzi dei nuovi casi e di morti per cancro si verificano nei paesi in via di sviluppo, dove l'incidenza è segnalata con ritmo di crescita continua e allarmante. Tali dati sono comprensibili se si tiene conto che l'OMS attribuisce a circa un terzo di tutte le morti per cancro una causa legata ai fattori di rischio modificabili, come il fumo, l'obesità, l’abuso di alcol e le infezioni. Tutte queste condizioni, combattute ormai da qualche tempo con un certo successo nei paesi sviluppati, non hanno ancora trovato una documentabile azione programmatica di prevenzione in quelli ancora in via di sviluppo. Differenze di ordine sanitario contribuiscono, inoltre, a spiegare l’epidemiologia specifica tra i Paesi. Si pensi al dato che molti tipi della malattia possono essere evitati con interventi di prevenzione, come lo screening del cancro del collo dell'utero, la vaccinazione contro le infezioni come l'epatite B e il papilloma virus umano. Ancora la diagnosi precoce come per il tumore del seno, del collo dell'utero e del colon-retto, può comportare anche il successo delle cure.
A tale proposito, l'OMS ha un programma di finanziamento per molti paesi in via di sviluppo fornendo informazioni e aiuti per pianificare la prevenzione e le strategie del trattamento. Anche l'American Society for Clinical Oncology ha annunciato l'intenzione di espandere la portata dei suoi programmi internazionali e di raddoppiare il loro finanziamento per aiutare ad affrontare il crescente onere globale del cancro.
L’ESMO (European Society for Medical Oncology), per sua parte, ha annunciato di sostenere la giornata mondiale per il cancro con l’intenzione di confermare, secondo un sogno ormai non più lontano, la realtà della medicina personalizzata per tutti i tipi di malattia e di malati. L'obiettivo è, infatti, quello di curare i pazienti in rapporto alle caratteristiche del tumore con terapie mirate e specifiche. La situazione attuale è, invero, quella di un’oncologia stratificata in grado di individuare e valutare gli obiettivi critici nel tumore per cercare di sviluppare farmaci intelligenti. In base alle moderne evidenze scientifiche, per gli oncologi emerge un doppio dovere: 1) accrescere la propria consapevolezza sui risultati attuali delle terapie mirate, sul loro elevato potenziale e sui requisiti necessari, 2) guidare i pazienti nella ricerca di sperimentazioni cliniche in cui i tumori possono essere meglio delineati per l’accesso ai nuovi trattamenti. È stata lanciata, quindi, dal WOF (World Oncology Forum) una campagna " Stop Cancer Now!" per riproporre, con l’obiettivo di ridurre del 25% entro il 2025 la mortalità mondiale, l'allarme sulla devastazione sempre più causata in tutto il mondo dal cancro.
I governi, per loro parte, dovranno intervenire per la cura dei tumori con specifici programmi di diagnosi precoce e di facilitato accesso alle indagini diagnostiche, ma anche alle cure palliative di dimostrata efficacia. Non devono, peraltro essere dimenticati ma sostenuti, coloro che convivono con il cancro.
Per sua parte, Umberto Veronesi, fondatore dell’Eso ha criticato la parzialità degli interventi degli studiosi e degli operatori nella lotta al cancro. Lo studioso, ha posto in rilievo la mancanza di una visione globale del problema e di un soggetto globale, un organismo di coordinazione della molteplicità degli interventi di lotta. Lo scienziato ha fatto, ib effetti, rilevare che la malattia rientra ancora tra quelle generiche non trasmissibili senza un ufficio specifico, neppure all'interno dell'OMS.
In conclusione, secondo Veronesi i ricercatori nello sviluppo dei farmaci, i clinici nell'anticipazione diagnostica e nelle strategie terapeutiche, i palliativisti nel controllo del dolore dovrebbero costituire un unico grande gruppo d’insieme nella lotta contro il cancro.
La campagna, comunque, programmata da un gruppo di esperti oncologi, leader e responsabili delle politiche e di altre istituzioni interessate, ha visto la collaborazione di società scientifiche e di stampa di tutto il mondo. In commemorazione della giornata, l'Empire State Building di New York è stato illuminato specificamente in arancione e blu.
Epidemiologia del rischio di cancro nell’obesità
Preoccupanti sono i dati che associano l’obesità allo sviluppo delle neoplasie maligne, tanto che alcuni dati la indicano al secondo posto, solo dopo il tabacco, nella classifica dei principali fattori di rischio. Pur tuttavia, i meccanismi molecolari alla base dell’aumento del rischio di cancro nell'obesità non sono ancora del tutto ben chiariti. In essa si sconvolge, invero, il ruolo dinamico degli adipociti nell'omeostasi energetica per effetto della conseguente infiammazione e alterazione delle adipochine, come la leptina e l’adiponectina. Inoltre, l’eccesso di adipe provoca cambiamenti secondari che possono anche favorire lo sviluppo del cancro e che riguardano la complessità dell'insulina e della deregolamentazione dei lipidi. La comprensione di questi legami molecolari può fornire, di fatto, una base importante per la programmazione delle strategie preventive e terapeutiche rivolte a ridurre, in una popolazione del mondo sempre più obesa, il rischio del cancro e la mortalità consequenziale. In verità, il nuovo concetto dell’epidemiologia molecolare ha permesso di disegnare un quadro d’integrazione nei rapidi progressi compiuti nello sviluppo di una vasta gamma di biomarcatori, aumentando la comprensione nelle popolazioni sui meccanismi della malattia. In effetti, l’epidemiologia molecolare, fiorita negli ultimi due decenni in un campo eccezionalmente ampio e diversificato, ha cambiato profondamente la nostra comprensione sulle cause di malattia. Ha utilizzato, di fatto, i progressi tecnologici collettivamente individuati come omiche, ossia: la genomica, la trascrittomica, la proteomica, la metabonomica. Così che, il loro impiego negli studi epidemiologici ha annunciato una rivoluzione nella progettazione, realizzazione e interpretazione degli studi sul nesso di causalità di malattia. Peraltro, l’epidemiologia molecolare ha riunito gli scienziati di tutte le discipline per interagire in grandi imprese, spesso utilizzando reti multinazionali, promuovendo consorzi con dimensioni e poteri d’indirizzo che hanno come sfida globale la riduzione o l’annullamento dei danni provocati dalle malattie.
Le evidenze, in effetti, indicano come negli ultimi venti anni il peso corporeo eccessivo, e meglio l’obesità, si associno a un aumentato rischio del cancro.
Quasi il 30% dei casi di questa drammatica malattia è, infatti, attribuibile all'eccesso del peso corporeo.
In questo modo, gli studi epidemiologici hanno fornito prove ormai convincenti che l'obesità aumenta il rischio per i tumori dell'esofago, dello stomaco, del colon, del pancreas, della mammella in post-menopausa, dell'endometrio e del rene. Pur tuttavia, l'entità dell'aumento del rischio varia secondo la sede tumorale. Ad esempio, per un aumento di 10 kg/m2 della BMI il rischio relativo è di circa 2,3 per l’adenocarcinoma dell'esofago, di 1.5 per il cancro del colon negli uomini, di 1.2 per il cancro del colon nelle donne, di 1,4 per il cancro al seno della donna in post-menopausa, di 2,9 per il cancro endometriale e maggiore di 1,5 per il cancro del rene. La dimensione dell’effetto sul cancro del pancreas è ancora incerta. Vi sono anche prove che l'obesità aumenta il rischio del cancro della colecisti, del melanoma maligno, dell’ovaio, della tiroide, del linfoma non-Hodgkin, del mieloma multiplo e della leucemia. Gli individui obesi, inoltre, hanno un rischio del 50% più alto di morire di cancro, rispetto ai loro omologhi di peso normale. Nell’ambito di quest’analisi si è anche appurato che per ogni 1% di riduzione della BMI, equivalente a una perdita di peso di circa 1 kg per un adulto di peso medio, si eviterebbe l'aumento effettivo dei casi di cancro di circa 100.000 nuovi casi di tumore.
C'è stata anche prova sufficiente dell’effetto di prevenzione dell’attività fisica. A tale proposito l’EPIC (European Prospective Investigation into Cancer and Nutrition) sta portando avanti la ricerca in questo campo per sviluppare e migliorare i metodi di valutazione dell'attività fisica, della composizione corporea e delle abitudini alimentari e anche per studiare le relazioni tra l’obesità, l’attività fisica e il rischio di cancro.
Quali relazioni tra obesità e cancro?
Per le possibili spiegazioni sulla stretta relazione tra l’obesità e il cancro, vi sono varie ipotesi e studi. L’eccesso di estrogeni, prodotto dal tessuto adiposo, potrebbe spiegare l’aumento del rischio del cancro al seno, all’endometrio e in altre sedi. Peraltro, gli obesi hanno spesso un aumento dei livelli d’insulina e dell’IGF-1 (insulin-like growth factor-1) nel sangue, condizione nota per favorire lo sviluppo di alcuni tumori. Vi sono ormai evidenze che riconoscono nel tessuto adiposo un obiettivo importante dell’azione del GH (Growth hormone) che stimola la lipolisi negli adipociti maturi e nei preadipociti primari, ma promuove l’adipogenesi nelle linee cellulari dei preadipociti. La PRL (prolactin) e l’ormone lattogeno placentare stimolano anche loro l’adipogenesi nelle linee cellulari dei preadipociti, ma hanno effetti lipolitici variabili e lipogenici nel tessuto adiposo maturo. Il GH agisce direttamente attraverso il suo recettore oppure sovraregolando l’IGF-I (insulin-like growth factor), mediatore fondamentale della proliferazione della differenziazione e della sopravvivenza dei preadipociti. A tal proposito, sono tornati utili i risultati degli studi clinici sul trattamento con il GH nei pazienti con suo deficit o con sindrome da sua relativa insensibilità. Sono possibili, difatti, studi per l’analisi del GH e dell’IGF, come pure le azioni in vivo dell’IGFBP (IGF-binding protein). Durante la differenziazione in vitro degli adipociti si realizzano cambiamenti del sistema GH / IGF con le relative vie di segnalazione e il loro impatto sulla crescita e sulla funzione del tessuto adiposo. Considerazioni cliniche includono anche gli effetti del GH e dell’IGF-I sul tessuto adiposo durante il trattamento del deficit di GH, le differenze nel sistema dell’IGF tra i depositi di tessuto adiposo viscerale e sottocutaneo e il recente ruolo emergente per il tessuto adiposo della regolazione dell'omeostasi del glucosio.
Attner B della Lund University, Sweden e collaboratori, per studiare come l'incidenza del cancro sia correlata al diabete, all’obesità o ai lipidi nel sangue, hanno studiato 19.756 casi di cancro abbinati a 147.324 controlli nei riguardi dell'età, del sesso e del domicilio (Cancer Causes Control. 2012; 23(5):769-77). La diagnosi del diabete, dell’obesità o della dislipidemia era formalizzata a 0-10 anni prima della diagnosi del cancro. Il diabete era significativamente più comune prima della diagnosi nei pazienti con tumore del fegato, del pancreas, del colon, del tratto urinario e della vescica. Nelle pazienti con cancro della mammella il diabete era diagnosticato a 0-4 anni prima. Un minor rischio di diabete si osservava nei pazienti con carcinoma della prostata. I risultati permanevano anche dopo aggiustamento per l'obesità e i lipidi elevati nel sangue. L'obesità era, comunque, significativamente più comune nei pazienti con tumore dell'endometrio, del colon e del rene. Nel cancro al seno in età superiore ai sessanta anni l'obesità concomitava alla diagnosi del cancro. I lipidi alti nel sangue erano significativamente più comuni nei pazienti con carcinoma ovarico e meno comuni in quelli con cancro al seno.
In conclusione, lo studio, secondo gli Autori, confermava in materia di comorbidità del cancro alcuni risultati precedenti, ma anche nuovi.
Per altra parte non bisogna dimenticare che le cellule adipose producono ormoni, le adipochine, che possono stimolare o inibire la crescita delle cellule. Per esempio, la leptina, che è più elevata nelle persone obese, sembra promuovere la proliferazione cellulare, mentre l’adiponectina, che è ridotta, può promuovere effetti opposti. Le cellule adipose possono anche avere effetti diretti e indiretti su altri regolatori della crescita del tumore, tra cui il mTOR (mammalian target of rapamycin) e l’AMP-activated protein chinasi.
Paz-Filho G dell’Australian National University, Canberra – Australia e collaboratori hanno in questo contesto riesaminato il ruolo di organo endocrino giocato dal tessuto adiposo in rapporto per l’appunto alle due adipochine più particolari e più studiate, la leptina e l’adiponectina, implicate di là dai loro ruoli tradizionali nell’omeostasi energetica, ma anche come mediatori dello sviluppo del cancro (Front Biosci. 2011; 16:1634-50). Gli Autori hanno esaminato, quindi, queste sostanze a proposito delle neoplasie della prostata, della mammella, del colon-retto, della tiroide, del rene, del pancreas, dell’endometrio e dell’esofago. Hanno anche tracciato il loro ruolo nell’orchestrare l'influenza dell'obesità nello sviluppo di queste neoplasie.
Peraltro, le persone obese hanno spesso anche un basso livello di condizione d’infiammazione cronica o subacuta, associata com’è noto, con un aumentato rischio di cancro. Altri possibili meccanismi possono risiedere nelle risposte immunitarie alterate, negli effetti sul sistema NF-κB (nuclear factor kappa-light-chain-enhancer of activated B cells) e nello stress ossidativo.
Peraltro, ormai da più parti si ritiene che il tessuto adiposo in eccesso comporti cambiamenti metabolici, come la riduzione delle HDL, l’aumento dei trigliceridi, l’ipertensione e l’insulino-resistenza. D’altro canto, il reflusso esofageo, la stessa ipertensione, l’insulino-resistenza e le alterazioni endocrine, tutte condizioni indotte dall’obesità, potrebbero contribuire all’aumento del rischio del cancro dell’esofageo, del rene, del colon-retto e della mammella. Inoltre, anche l’infiammazione associata all'obesità contribuisce, di certo, alla progressione del cancro in diversi organi. Pur tuttavia, non sono stati ancora delucidati compiutamente i meccanismi alla base dell’associazione tra obesità e cancro, pur essendone stati proposti diversi e specifici per sede. L'evidenza che l'espressione e / o l’attività della FASN (Fatty acid synthase), che catalizza la sintesi degli acidi grassi, sono elevate nel cancro del seno, del colon-retto, della prostata, dell'endometrio, dell'ovaio e della tiroide è a favore dell’ipotesi che questo enzima risponderebbe all’esaltata biosintesi degli acidi grassi nelle cellule tumorali e che svolgerebbe un ruolo essenziale per generare le membrane cellulari durante la loro proliferazione. Peraltro, l'elevazione dell’espressione neoplastica della FASN si ricongiunge all’evidenza dell’importante ruolo del metabolismo dell’acido grasso arachidonico polinsaturo sull’infiammazione e sulla progressione del cancro, attraverso la via della COX (cicloossigenasi). In effetti, in diversi tumori solidi i livelli della COX-2 risultano elevati e la sua espressione si associa, in genere, a una ridotta sopravvivenza dei pazienti. A tale proposito, una gran mole di studi ha finora indicato che l'uso regolare dei FANS, tra cui l'aspirina per un periodo dai dieci ai quindici anni, ridurrebbe nel 40 -50% dei casi il rischio relativo di sviluppo del cancro del colon-retto.
Peter M Rothwell dell’University of Oxford, UK e collaboratori, proprio in base alla riduzione a lungo termine dell'incidenza di alcuni adenocarcinomi per merito dell'aspirina assunta quotidianamente con effetti sulla mortalità anche dopo pochi anni, hanno considerato tale dato suggestivo per un’inibizione alla crescita o alle metastasi (The Lancet, Volume 379, Issue 9826, Pages 1591 - 1601, 28 April 2012). Gli Autori hanno, così, stabilito la frequenza delle metastasi a distanza nei pazienti che avevano sviluppato il cancro durante gli studi di aspirina giornaliera rispetto ai controlli. L’analisi ha incluso tutti e cinque i grandi studi per la prevenzione di eventi vascolari nel Regno Unito, randomizzati con aspirina ≥ 75 mg/die verso i controlli. Dei 17.285 partecipanti alla sperimentazione, 987 presentavano la diagnosi di un nuovo cancro solido durante i 6,5 anni (SD 2.0) di follow-up medio. Il gruppo con aspirina mostrava una riduzione del cancro con metastasi a distanza (tutti i tumori, hazard ratio [HR] 0,64, 95% IC 0,48 -0 · 84, p = 0.001; adenocarcinoma, HR 0.54, 95% IC 0,38 -0 · 77, p = 0,0007; altri tumori solidi, HR 0,82, 95% IC 0,53 -1 · 28, p = 0.39), dovuta principalmente a una diminuzione proporzionale degli adenocarcinomi con malattia metastatica rispetto a quella locale (odds ratio 0,52, 95% IC 0,35 -0 · 75, p = 0,0006). L'aspirina riduceva nei pazienti senza metastasi iniziali il rischio degli adenocarcinomi con questa complicazione al momento della diagnosi iniziale (HR 0,69, 95% IC 0,50 -0 · 95, p = 0.02) e il rischio di metastasi al successivo follow-up (HR 0 · 45, 95% IC 0,28 -0 · 72, p = 0.0009). Tutto ciò particolarmente nei pazienti con tumore del colon-retto (HR 0,26, 95% IC 0,11 -0 · 57, p = 0,0008) e che erano rimasti in studio di trattamento fino o anche dopo la diagnosi (HR 0,31, 95% IC 0,15 -0 · 62, p = 0.0009). L’assunzione di aspirina riduceva anche la morte per il cancro in quei pazienti che avevano sviluppato l’adenocarcinoma, in particolare in quelli senza metastasi alla diagnosi (HR 0.50, 95% IC 0,34 -0 · 74, p = 0,0006). Di conseguenza, l'aspirina riduceva il rischio complessivo dell’adenocarcinoma fatale nei soggetti in studio (HR 0.65, 95% IC 0,53 -0 · 82, p = 0,0002), ma non il rischio di altri tumori letali (HR 1 · 06, 95% IC 0,84 -1 · 32, p = 0.64, differenza, p = 0.003). Gli effetti erano indipendenti dall'età e dal sesso, ma il beneficio assoluto si riscontrava nei fumatori. In effetti, la formulazione a lento rilascio dell’aspirina a basso dosaggio, progettata per inibire le piastrine, ma con poca biodisponibilità sistemica, si rendeva efficace quanto le dosi più alte. Il fatto, quindi, che l'aspirina previene le metastasi a distanza potrebbe spiegare la riduzione precoce dei decessi per cancro negli studi con aspirina giornaliera, rispetto ai controlli. Tale rilievo suggerirebbe, secondo gli Autori, che l'aspirina potrebbe essere di aiuto nel trattamento di alcuni tipi di cancro anche per l'intervento farmacologico specifico nel prevenire le metastasi a distanza.
La cascata degli eventi nel collegamento tra obesità e cancro
Il tessuto adiposo è riconosciuto tradizionalmente come l’elemento del corpo che fornisce energia per la crescita, la riproduzione e la funzione immunitaria, ma secerne e riceve anche diverse molecole di segnalazione che coordinano, per risposta a condizioni ecologiche, la ripartizione dell’energia tra queste funzioni. Bisogna certamente porre attenzione ai rilievi che associano l'obesità a diverse malattie croniche, ma senza dimenticare le molteplici funzioni benefiche del tessuto adiposo. È importante, infatti, porre l’accento che molti rilevanti spunti ecologici agiscono sulla crescita e sul fisico dell’uomo e che l’adiposità è come risposta nell’ambito di una strategia di contro bilanciamento del rischio. Il gran numero dei singoli alleli associati con il tessuto adiposo illustra la sua integrazione con diverse vie metaboliche. Tuttavia, la variazione fenotipica con l’età, con il sesso, con lo stato etnico e sociale si associa a diverse strategie per la conservazione e l'uso dell'energia. L’adiposità, quindi, rappresenta uno strumento fondamentale di flessibilità fenotipica all'interno e attraverso le generazioni, consentendo una coerente storia di strategia di vita di fronte alla stocasticità demografica, ambientale ed ecologica. La sensibilità delle vie metaboliche ai numerosi spunti ecologici rende, peraltro, la nostra specie abbastanza vulnerabile alla manipolazione delle forze economiche globalizzate.
È noto oramai come l'obesità si caratterizzi per un basso grado d’infiammazione sistemica cronica con un aumento delle concentrazioni plasmatiche delle citochine e delle proteine infiammatorie della fase acuta. Questo basso livello d’infiammazione cronica rappresenta conseguentemente una delle principali cause dell’insulino-resistenza costituendo, quindi, un fattore di rischio per il diabete mellito tipo 2. La causa dell’infiammazione del tessuto adiposo è ancora oggetto di dibattito, richiedendo altri chiarimenti. È stato anche ipotizzato che la carenza di vitamina “D” sia alla base di questa predisposizione e che gli individui sviluppino, così, l’infiammazione del tessuto adiposo. Ciò comporterebbe il trattamento preventivo della vitamina per evitare soprattutto il diabete di tipo 2 e l’aumentato rischio delle malattie cardiovascolari e di alcuni tipi di cancro. Le evidenze, anche recenti, suggeriscono, in verità, che questa infiammazione sistemica è causata, almeno in parte, dall’infiammazione del tessuto adiposo. In tal modo, la ricerca sperimentale sui modelli murini dell’obesità ha suggerito che l’aumento della massa grassa si associa con una sua maggiore infiltrazione di macrofagi, di cellule T e di altri leucociti con cambiamento fenotipico di queste cellule. Sono in corso, pur tuttavia, studi per la conferma di questi dati anche nell’uomo e per giustificare, quindi, l'aumento del rischio delle malattie cardiovascolari e di alcuni tipi di cancro associati con l'obesità.
Weisberg SP della Columbia University, New York e collaboratori hanno voluto caratterizzare i cambiamenti che si verificano nel tessuto grasso nell’adiposità crescente. Ciò come approfondimento del dato che l'obesità altera la funzione endocrina e metabolica del tessuto adiposo con un aumento del rilascio degli acidi grassi, degli ormoni e delle molecole proinfiammatorie, determinanti per le consequenziali complicazioni (J Clin Invest. 2003 December 15; 112(12): 1796–1808). Gli Autori hanno, così, profilato l’espressione trascrizione nel tessuto adiposo perigonadale di topi Ay (agouti) e Lepob obesi, in cui adiposità varia a secondo del sesso, della dieta e delle mutazioni correlate all'obesità. L'espressione di 1.304 trascritti correlava in modo significativo con la massa corporea. Tra i cento geni più significativamente correlati, il 30% delle proteine codificate erano caratteristiche dei macrofagi e si associavano positivamente con la massa corporea. Le analisi immunoistochimiche del tessuto adiposo perigonadale, perirenale, mesenterico e sottocutaneo rivelavano che la percentuale delle cellule esprimenti il marcatore F4/80 (F4/80 +) dei macrofagi era significativamente e positivamente correlata con la dimensione degli adipociti e con la massa corporea. Relazioni simili si dimostravano nel tessuto adiposo sottocutaneo umano colorato per l'antigene macrofagico CD68. Peraltro, gli studi sul trapianto del midollo osseo e sulla quantificazione del numero dei macrofagi nel tessuto adiposo di topi Csf1op/op (colony-stimulating factor 1), deficienti in macrofagi, suggeriscono che queste cellule F4/80 + sono macrofagi del tessuto adiposo CSF-1 dipendenti, derivate dal midollo osseo. Le analisi dell’espressione delle popolazioni cellulari dei macrofagi e non, isolate dal tessuto adiposo, dimostravano che i primi erano responsabili di quasi tutta quella del TNF-α e in modo significativo di quella dell’iNOS (inducible nitric oxide synthase) e dell’IL-6 (interleukin-6).
In conclusione, il numero dei macrofagi del tessuto adiposo aumentava nell’obesità e partecipava ai percorsi infiammatori attivati nel tessuto adiposo.
Sheng Xia della Cornell University, Ithaca - New York e collaboratori, proprio sulla base dell’attivazione delle cellule immunitarie, compresi i macrofagi e le cellule CD8 + T, nel contributo significativo al progresso dell'obesità e delle sue complicanze mediche, hanno voluto esplorarne ulteriormente la regolazione in vivo (J Biol Chem. 2011 July 1; 286(26): 23591–23599). Lo studio ha riguardato un gruppo di cellule mieloidi immature con marcatori cellulari di superficie Gr-1 + CD11b +, altamente arricchiti nei tessuti periferici, come il fegato e l’adipe nel soggetto obeso. La sottoregolazione di queste cellule negli animali obesi aumentava in modo significativo l'infiammazione e alterava la sensibilità all'insulina e la tolleranza al glucosio. Invece, il loro trasferimento adottivo riscuoteva l'effetto opposto. Meccanicamente, si dimostrava che in condizioni di obesità le cellule Gr-1 + sopprimevano la proliferazione e inducevano l'apoptosi delle T CD8 +. Erano, altresì, in grado di predisporre la differenziazione dei macrofagi in insulinosensibilizzanti, in alternativa a quelli attivati M2. Nel suo insieme lo studio, secondo gli Autori, avrebbe dimostrato che le cellule mieloidi immature fornivano la piattaforma di controllo e di contrappeso per contrastare cellule immunitarie proinfiammatorie nel fegato e nel tessuto adiposo durante l'obesità, onde evitare evidenti risposte immunitarie.
Hursting SD e Hursting MJ dell’University of Texas, Austin – USA, considerando che l'obesità spesso si evidenzia come sindrome metabolica ed è un fattore di rischio stabilito per molti tumori, hanno riportato una recensione sintetizzando gli elementi di prova sui principali meccanismi biologici alla base del legame tra queste patologie (Arterioscler Thromb Vasc Biol. 2012; 32(8):1766-70).
I percorsi interconnessi, con particolare riguardo ai fattori di crescita, quelli dell’infiammazione e dell’integrità vascolare, rappresentano, invero, i possibili obiettivi meccanicistici per interrompere questo legame.
Per altro verso, le cellule dei mammiferi richiedono un adeguato controllo trascrizionale del ciclo cellulare al fine di negoziare i complessi processi di sintesi del DNA, la duplicazione dei cromosomi e la risoluzione dei problemi topologici di duplicazione. Il mancato mantenimento di questo sviluppo mette a repentaglio la sopravvivenza delle cellule e favorisce la malignità. In questa connessione sono state osservate le proteine che contengono un bromodominio, le quali regolano la struttura cromatinica e l’epigenetica. È noto che il bromodominio proteico funziona come modulo di legame a istoni modificati, deputato a legare selettivamente le lisine acetilate. È un motivo altamente conservato di centodieci aminoacidi, dotato di quattro α-eliche anti-parallele. Definito per la prima volta nella proteina Drosophila brahma, ha da qui derivato il suo nome. Si trova, peraltro, in quasi tutte le HAT (histone acetyltransferases), nei coattivatori trascrizionali e nei componenti della cromatina associata ai complessi multi proteici. In definitiva, la conoscenza della composizione dinamica dei complessi proteici del bromodominio ha apportato maggiore chiarezza sui meccanismi di regolazione genica, sul controllo del ciclo cellulare e sulla malignità. In genere ogni proteina si lega selettivamente solo a un particolare residuo istonico modificato. Il bromodominio è stato individuato in proteine che interagiscono con la cromatina, come i fattori di trascrizione, le acetilasi istoniche e i complessi di rimodellamento del nucleosoma SWI / SNF (SWItch/Sucrose NonFermentable). Nell’uomo sono stati riconosciuti cinquantasei bromodomini codificati in quarantadue proteine. Essi nel DNA si trovano strettamente in relazione ai membri della superfamiglia delle elicasi correlate all’associata matrice dello SWI / SNF, actino-dipendente, regolatore della cromatina, dello SMARCA2, noto anche come brahma, BRM e SNF2α, e dello SMARCA4, noto anche come BRG1 e SNF2β. I due SMARCA2 e SMARCA4 sono le fondamentali subunità catalitiche, che si escludono a vicenda, dell’ATPasi di un complesso SWI / SNF che regola lo stato della cromatina. Il bromodominio si trova anche in molti regolatori trascrizionali e di sviluppo che funzionano attraverso la modificazione degli istoni e il rimodellamento dei nucleosomi. Si tratta di regolatori HAT (authentic histone acetyltransferases), come la CBP (CREB-binding protein) e il TAF1 (TBP-associated factor 1), noto anche come CCG1 e TAFII250. Questi domini sono tra loro collegati e disposti in tandem nelle proteine che contengono due bromodomini, come le BET. Quanto sin’ora riportato indica che le proteine BET svolgono un ruolo cruciale nella regolazione della trascrizione genica. Difatti, attraverso l'assunzione di proteine formano complessi che modificano la cromatina. In effetti, le proteine istoniche cromatinoregolatorie sono da qualche tempo state implicate nel cancro. Oggi la deregolamentazione epigenetica della trascrizione è giudicata tanto importante per la cancerogenesi quanto la mutazione genetica. Inoltre, le proteine della famiglia BET (bromodomain and extraterminal) sono mediatrici chiave per il montaggio della trascrizione del complesso P-TEFb (positive transcription elongation factor b), un evento necessario per l'inizio dell’allungamento della trascrizione.
In particolare, le BET hanno dimostrato di essere implicate nel cancro, dove possono essere espresse come fusioni di oncogeni maligni insieme al NUT (nuclear protein in testis), una proteina con funzione ancora sconosciuta che causa carcinomi molto aggressivi e scarsamente differenziati a principale sede di origine nella linea mediana del corpo, come la testa, il collo e il mediastino.
I requisiti spaziali per il reclutamento, da parte delle proteine BET del P-EFb sulla cromatina, rimangono ancora fino a oggi incerti e non sono chiari quali componenti di queste proteine siano direttamente implicati. La migliore comprensione di tali interazioni farà, di certo, luce sul loro ruolo nella trascrizione, fornendo le informazioni di vitale importanza per l’interpretazione delle malattie e la progettazione delle più efficaci terapie. Le proteine BET dei mammiferi sono, quindi, una classe di coregolatori trascrizionali contenenti una doppia serie di motivi di bromodominio, reciprocamente connessi, e un dominio extraterminale. Assumono importanza nel controllo del network dei geni, si legano alle lisine acetilate negli istoni della cromatina nucleosomale, reclutano gli enzimi della cromatina di modificazione per i promotori bersaglio e la funzione, a seconda del contesto, come coattivatori e corepressori dell’espressione genica. Nuove piccole molecole inibitrici sono state recentemente sviluppate per interrompere l’interfaccia del legame tra il bromodominio e i gruppi acetilati della lisina. Questi elementi hanno notevole potenza, selettività e sono ben tollerati. Essi sono stati recentemente utilizzati come agenti antitumorali e anti-infiammatori.
In effetti, gli inibitori delle proteine BET hanno dimostrato proprietà anti-infiammatorie. Infatti, le proteine BET BRD2, BRD3 e BRD4 regolano l'assemblaggio di acetilazione della cromatina dipendente dai complessi dell'istone che regolano l’espressione del gene dell’infiammazione. Un composto I-BET, strutturalmente simile all’JQ1, sostanza che ha preso il nome del chimico omonimo, dimostra, infatti, proprietà anti-infiammatorie. Studi sperimentali sui topi hanno evidenziato i rapporti tra le proteine BET e l’infiammazione e il fenotipo murino ha fornito un modello per gli esseri umani in cui l'obesità, non inevitabilmente associata al rischio cardiometabolico, non può essere considerata interamente dannosa. Questi soggetti MHO (metabolically healthy obese), corrispondenti a una percentuale valutata negli Stati Uniti a circa il 25% dei totali, dimostrano una sensibilità all'insulina conservata e una tolleranza glucidica eccellente, ma soprattutto un profilo infiammatorio ridotto. Hanno, difatti, un aumento meno marcato di PCR, di TNF e di altre citochine proinfiammatorie. Hanno per tutto questo minori complicazioni, come l’insulinoresistenza, la sindrome metabolica, l’ipertensione, il diabete di tipo 2 e le malattie cardiovascolari. Questi soggetti sono anche protetti da tutte le cause di mortalità di cancro rispetto ai soggetti insulinoresistenti. È interessante ipotizzare che i soggetti MHO possano avere alleli dei geni BET, in particolare BRD2, con protezione nell’obesità contro una disfunzione metabolica o un cancro. Per altro canto, si è dimostrata anche la coattivazione dei geni proinfiammatori che dipendono dalla trascrizione NF-kB attraverso l'interazione con il RELA acetilato. Bisognerà ottenere una completa conoscenza sul ruolo reciproco del BRD2, BRD3 e BRD4 e sulla modalità di coattivazione del NF-kB nella cooperazione con il complesso SWI / SNF nella regolazione delle risposte di trascrizione dei geni che codificano le citochine importanti proinfiammatorie, come il TNF e l’IL-6. Questi dati sono, di certo, rilevanti per il potenziale legame tra l'infiammazione cronica e l’aumentato rischio del cancro. È possibile, difatti, che l'infiammazione promuova alcuni tumori associate all'obesità nella sede d’infiammazione del tessuto adiposo bianco nei soggetti obesi insulinoresistenti. E a tale proposito, è interessante notare come la caratteristica infiammazione intestinale della malattia di Crohn sia fortemente correlata con il cancro colorettale. Peraltro sotto tale profilo, il ruolo ancora non del tutto risolto dell’infiammazione cronica e quello della disfunzione metabolica nell'obesità associata ai tumori potrebbero aprire la strada a nuovi farmaci, come agli inibitori delle BET. In definitiva, le funzioni proteiche delle BET interesserebbero l’adipogenesi, la produzione delle citochine infiammatorie, il controllo del ciclo e i programmi di sviluppo cellulare, processi in realtà profondamente interconnessi perché condividono un numero limitato di attori epigenetici. Pur tuttavia, per la segnalazione della trasduzione in ciascun caso e per le risposte cellulari specifiche, sono necessari i fattori di trascrizione adipogenici come il PPARγ, quelli infiammatori come il NF-kB, del ciclo cellulare come le E2F e specifici di ceppo come il PU.1 e il TBET.
Anna C. Belkina e Gerald V. Denis della Boston University School of Medicine – USA hanno esaminato gli sviluppi e hanno discusso le implicazioni delle BET per le loro possibili azioni contro il cancro (Nature Reviews Cancer 12, 465-477, July 2012).
D’altra parte, alcune interazioni coinvolgono la corepressione trascrizionale, come la trascrizione insulinica, la differenziazione controllata nel tessuto adiposo dal PPARγ (peroxisome proliferator-activated receptor-γ) e quella del GATA1 (anche noto come erythroid transcription factor) nel controllo ematopoietico.
La corepressione trascrizionale dei loci specifici è un processo attivo che richiede l'assunzione dei complessi repressori. Nel caso del PPARγ è abilitata attraverso l’associazione del BRD2 con il RXR, che è noto per eterodimerizzare con il PPARγ. La rimozione mediante l’ablazione genetica del BRD2 promuove la trascrizione del network adipogenico, analogamente al trattamento con tiazolidinedione. Peraltro, piccole molecole inibitrici delle proteine dovrebbero produrre un risultato simile.
Altre interazioni coinvolgono la coattivazione trascrizionale, come l'attivazione dei geni che promuovono la progressione del ciclo cellulare. A tale proposito, intervengono il MYC (termine derivato dal myelocytomatosis viral oncogene) e le proteine E2F. Per la sintesi delle citochine proinfiammatorie agisce più particolarmente il NF-kB (nuclear factor-κB), mentre per la regolazione dei geni cellulari il P-TEFb (The positive transcription elongation factor).
Comunque, la gamma completa di coinvolgimento delle proteine BET nel cancro è ancora da stabilire completamente. L'interazione del BRD4 con il P-TEFb e del TAF1 con la proteina E2 dell’HPV (human papillomaviruses), associato al rischio del cancro cervicale, porta l'attenzione sulla relazione tra il BRD4 dell’ospite e le proteine codificate dal virus, importanti per il controllo trascrizionale e il cancro. È importante rilevare che nelle cellule infettate dall’HIV, il fattore trascrizionale Tat dell’uno compete con il BRD4 dell’ospite per il legame del P-TEFb, presente sul terminale del virus. Tutto ciò per il controllo della trascrizione insieme all’attività HAT e del complesso
SWI / SNF.
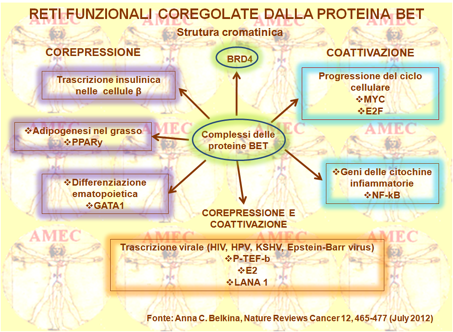
Peraltro, la trascrizione e la replicazione dei virus latenti sembrano sfruttare la capacità della proteina BET, sia per la corepressione sia per la coattivazione, secondo le esigenze del virus mediante il P-TEFb, lo human papilloma virus (HPV) E2 protein, la proteina E2 o il Kaposi's sarcoma-associated herpesvirus (KSHV) latency associated-nuclear antigen 1 (LANA1) protein. Dati recenti coinvolgono la proteina BRD4 (Bromodomain-containing protein 4) anche per il mantenimento della struttura di ordine superiore della cromatina.
Derick Okwan-Duodu dell’Emory University School of Medicine, Atlanta e collaboratori hanno pubblicato una revisione sullo sviluppo disfunzionale delle cellule ematopoietiche durante la carcinogenesi (Am J Cancer Res 2013;3(1):21-33).
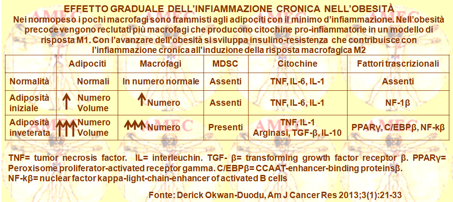
Gli Autori hanno descritto come le cellule della linea mieloide, sotto forma di MDSC (myeloid derived suppressor cells) e alternativamente di macrofagi polarizzati M2, possano influenzare quasi tutti i tipi di tumori mediante il controllo dei diversi aspetti dell’immunosoppressione, dell'angiogenesi, della proliferazione cellulare, della crescita e delle metastasi.
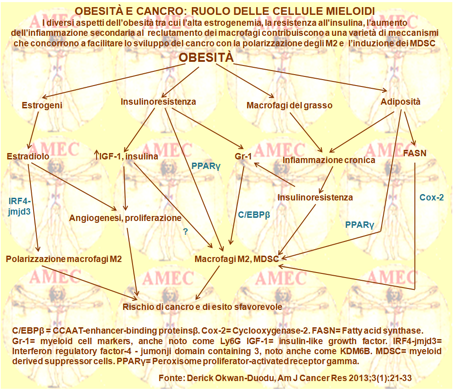
Gli Autori, pur segnalando il non ben descritto rapporto tra questi attori del sistema immunitario e l'obesità, hanno esaminato i meccanismi potenziali attraverso cui i diversi aspetti dell’obesità, come l’insulinoresistenza, l’aumento degli estrogeni, il basso grado d’infiammazione cronica possono fondersi per la promozione dell’induzione dei MDSC e della polarizzazione dei macrofagi M2, facilitando così lo sviluppo del cancro. In effetti, dalla comprensione dettagliata dell’interazione tra obesità e immunosoppressione mediata mieloide si possono identificare nuove strade per il targeting terapeutico, con l'obiettivo di ridurre la sfida che l’obesità presenta verso i migliori risultati contro il cancro.
Cellule progenitrici derivate dal tessuto adiposo e cancro
Sotto altro aspetto, bisogna considerare che il corso dei vari processi patologici dipende dal reclutamento delle cellule staminali e da quelle progenitrici in parte differenziate.
A tale proposito, Yan Zhang dell’University of Texas at Houston, United States hanno riportato una dettagliata revisione sulle condizioni e sugli effetti dell’elevata circolazione sistemica dei precursori ematopoietici ed endoteliali, popolazioni cellulari ritenute sempre più implicate nella progressione delle varie malattie (World J Stem Cells 2010 October 26; 2(5): 103-113). Negli ultimi anni, difatti, è stata data sempre maggiore rilevanza clinica alla mobilitazione delle cellule staminali / progenitrici. Si è, così, cercato di identificare i fattori di tale fenomeno, inizialmente per il suo potenziale utilizzo nella medicina rigenerativa. Le EPC (Endothelial progenitor cells), che danno luogo alla maturazione delle CE (endothelial cells), rappresentano un’altra popolazione cellulare clinicamente importante. Difatti, la formazione dei nuovi vasi o la riparazione o la patologia di un tessuto dipendono per l’angiogenesi e il sostegno del microcircolo dalla proliferazione locale delle CE. È noto, ormai, che, oltre all’angiogenesi, il reclutamento delle cellule progenitrici circolanti dal midollo osseo nei vasi sanguigni avviene con la vasculogenesi nell’adulto in risposta all'ipossia e all'infiammazione. Questa nuova concezione, invero, ha cambiato negli studiosi la visione delle modalità della composizione vascolare dei tessuti patologici. L’aumento dei livelli circolanti delle EPC, in effetti, è stato associato, per il beneficio della loro mobilitazione nei tessuti ischemici, a un ridotto rischio di morte cardiovascolare. Nella vascolarizzazione dei tumori, invece, il mimetismo endoteliale giocherebbe un ruolo importante. Peraltro, alcune popolazioni di cellule circolanti, ad eccezione delle CE e delle EPC, sono state recentemente implicate a sostegno della vasculogenesi tumorale. Le TADC (Tumor-associated dendritic cells), una nuova popolazione leucocitaria che esprime sia le DC (Dendritic-Cell) sia i marcatori endoteliali, hanno mostrato di partecipare alla composizione della neovascolarizzazione del carcinoma ovarico. Le RBCCR (Recruited bone marrow-derived circulating cells), che esprimono i VEGFR1 (Vascular endothelial growth factor) ma non i VEGFR2, vengono trasportate in vari organi dove s’impegnano nella neovasculogenesi. Inoltre, si è dimostrato che, similarmente alle RBCCs, una popolazione di TEM (TIE2-expressing monocytes) viene impiegata nei siti tumorali promuovendo, in un modo paracrino dopo aver aderito ai vasi sanguigni di nuova formazione, l'angiogenesi tumorale. Alcune o tutte queste popolazioni cellulari CD45 + circolanti proangiogeniche possono essere identiche alle cellule precedentemente descritte come fibrociti. È interessante notare, a tal proposito, che i fibrociti, essendo di origine mieloide, sono stati proposti in base alla loro differenziazione in vivo in adipociti, come i progenitori delle cellule mesenchimali. Peraltro, negli ultimi anni è stato riconosciuto alle MSC (mesenchymal stromal cells) un importante ruolo potenziale in un certo numero di condizioni patologiche. Isolate in origine dallo stroma del midollo osseo e chiamate sulla base della loro morfologia CFU-F (fibroblast colony-forming units), hanno dimostrato la capacità di differenziarsi nelle cellule delle linee mesenchimali, quali osteoblasti, condrociti e adipociti. Per questo, quindi, sono state chiamate cellule staminali mesenchimali. Inoltre, ulteriori studi hanno rivelato in vari organi che le MSC, mantenendo l'integrità vascolare come periciti, hanno anche una funzione di cellule perivascolari. Con l’invecchiamento sembra ridursi la capacità di risposta delle cellule progenitrici midollari agli stimoli di mobilitazione, cui consegue un diminuito impegno delle cellule del midollo osseo alla riparazione delle lesioni. Pur tuttavia, gli studiosi incominciano già a individuare il ruolo di altri organi come fonte di cellule progenitrici stromali. Ricerche sperimentali sui roditori, in effetti, hanno dimostrato che il WAT (white adipose tissue) può assumere questa funzione nel corso della sua espansione sino all’obesità con l’ipertrofia degli adipociti e con la loro iperplasia risultante dalla proliferazione dei progenitori. Difatti, nello SFV (stromal/vascular fraction) del WAT sono stati identificati progenitori multipotenti. Ciò nonostante, oltre agli adipociti il WAT contiene anche AEC (adipose endothelial cells), ASC (adipose stromal cells) perivascolari, ma anche cellule ematopoietiche, come macrofagi e linfociti. Diversi studi hanno dimostrato che questi progenitori mesenchimali corrispondono ad ASC CD34 +, CD45-, CD31-. Questi elementi nello SVF comprendono, invero, la maggioranza delle cellule e mostrano una multipotenzialità e capacità di proliferazione paragonabili alle MSC del midollo osseo, pur con chiare e uniche caratteristiche. Peraltro, coerentemente con il ruolo specifico dei depositi di grasso in patologia, il contenuto e le proprietà delle cellule sono stati rilevati differenziali tra quello viscerale e quello sottocutaneo. La neovascolarizzazione rappresenta un processo basilare nella progressione del cancro e nelle sue fasi che coinvolgono la crescita, l’invasione e le metastasi. La vasculogenesi coinvolge, invero, l'infiammazione associata all’infiltrazione delle cellule endoteliali ed ematopoietiche. In effetti, i livelli delle CPC (circulating progenitor cells) e delle EC mature sono elevati nei tumori umani. Peraltro, le EC circolanti attecchiscono nel sistema vascolare del tumore, suggerendo un loro possibile ruolo nella progressione della malattia, come per le varie popolazioni leucocitarie. Di poi, poiché i tumori secernono fattori che causano l’ipossia e l'infiammazione, è stato ipotizzato che anche le MSC possano essere reclutate dai tumori. In effetti, nei pazienti oncologici è stata rilevata un’elevata circolazione di CFU-F.
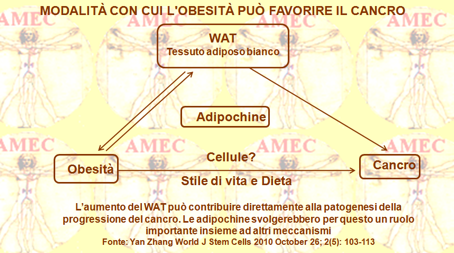
In ultima analisi, bisogna ribadire che l’individuazione dei fattori che possono influenzare il decorso clinico del cancro rappresenta, di certo, una tappa fondamentale per la strategia d’approccio alla malattia e per la sua gestione. L'obesità, certamente, è ormai uno dei fattori più importanti da considerare, perché in progressiva e ampia diffusione.
Peraltro, la diversità di distribuzione del grasso corporeo tra uomini e donne offre anche una spiegazione alle differenze epidemiologiche dell’associazione dell’obesità con alcuni tipi di cancro. Negli uomini, difatti, l’accumulo di adipe è caratterizzato da un grado relativamente elevato del gasso viscerale rispetto alle donne che mostrano, invece, un aumento del grasso sottocutaneo alle anche. Per di più, la fisiopatologia sottostante l'associazione tra obesità e cancro deve risiedere in fattori genetici e nell’errato stile di vita, come la dieta non salutare e la ridotta attività fisica. L’iperinsulinemia deve anche rappresentare, di certo, un sottostante meccanismo biologico per le associazioni osservate. Al contrario, la restrizione energetica e il suo conseguente effetto di riduzione dell’insulinemia avrebbero dimostrato nei modelli animali d’inibire la carcinogenesi. L’iperinsulinemia, peraltro, oltre ai suoi particolari effetti di promozione sulla crescita, aumenta l’espressione degli IGF (insulin-like growth factors), aumentando la loro biodisponibilità attraverso la diminuita sintesi delle IGFBP-1, IGFBP-2 e IGFBP-3 (IGF-binding proteins). In aggiunta al loro importante ruolo sulla crescita e allo sviluppo normale, gli IGF-1 e IGF-2, attraverso azioni autocrine paracrine ed endocrine, sarebbero in grado di promuovere la proliferazione delle cellule tumorali. Di poi, il recettore IGF-1 media l’attività proliferativa degli IGF. Peraltro, studi in vitro ed epidemiologici hanno dimostrato che gli estrogeni endogeni ed esogeni riducono i livelli sierici degli IGF-1. In definitiva, in ragione del fatto che l'obesità rappresenta uno stato di espansione del WAT, bisogna considerare plausibile il suo collegamento con il cancro e la sua progressione. IL WAT, di fatto, si è rivelato un potente organo endocrino capace di secernere e immettere in circolo vari fattori di crescita come l’IGF-1, l’IGFBP e il TGF-β, ma anche citochine, come il TNF-α e interleuchina-6) e ormoni, come la leptina. L'espressione di queste adipochine aumenta nell'obesità e compromette il metabolismo lipidico, la sensibilità all'insulina, il sistema alternativo del complemento, l'emostasi vascolare, l'angiogenesi e la regolazione del bilancio energetico. In effetti, alcune di queste adipochine hanno dimostrato di favorire il cancro in vari animali e in modelli in vivo. Per esempio, l’interleuchina-6 si è vista fortemente legata ai cancri del colon-retto associati all’infiammazione e all’IBD (inflammatory bowel disease). Pertanto, i segnali del sistema endocrino / paracrino da parte del WAT potrebbero essere alla base del meccanismo con cui i disordini metabolici correlati all'obesità conducono al cancro. In relazione alla notevole potenza biologica di presenza nel WAT della popolazione dei progenitori cellulari, viene da ipotizzare che la stessa possa essere spinta a mobilizzarsi spontaneamente per risposta a segnali patologici per essere reclutata nei siti di malattia e influenzarne la progressione. Queste cellule possono, per esempio, servire come extra CAF (cancer-associated fibroblasts) di riserva nei pazienti oncologici obesi. Il gruppo di Yan Zhang hanno, in effetti, proposto che le MSC possano venire mobilitate dal WAT (ASC) negli obesi in risposta a segnali tumorali ed essere reclutate per la vasculogenesi del tumore. Poiché gli adipociti sono drammaticamente elevati negli obesi, gli Autori hanno anche ipotizzato che un numero elevato di cellule derivate dal WAT vengano eventualmente mobilitate e reclutate dal tumore nei pazienti, spiegando meglio l’associazione tra l’obesità e la progressione del cancro.
A tale proposito, sono ormai disponibili diversi dati di studi sperimentali sugli animali che indicano come le cellule derivate dal WAT tendano a essere reclutate nei tumori con un’infiltrazione sia endoteliale sia di linee stromali in diversi compartimenti.
Lo stesso Yan Zhang e collaboratori, sempre per meglio chiarire le connessioni fisiopatologiche tra cancro e obesità, hanno in seguito dimostrato che questa malattia facilita la crescita tumorale nei topi indipendentemente dalla dieta concorrente, suggerendo un effetto diretto dell’eccesso del WAT (white adipose tissue). In effetti, una volta trapiantate nei topi, le ASC (adipose stromal cells) potevano servire come progenitrici perivascolari degli adipociti che promuovevano la crescita del tumore. Forse in tal modo aiutavano a spiegare il legame che unisce l'obesità al cancro. Gli Autori sviluppando questa ipotesi, hanno, così, dimostrato che le ASC erano espanse nell’obesità e in spostamento dal WAT endogeno nei tumori in diversi modelli murini di cancro.
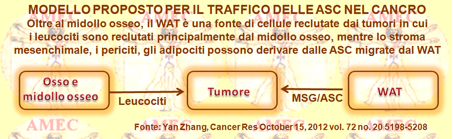
Sorprendentemente il confronto tra le popolazioni di cellule circolanti e infiltranti il tumore in topi magri e in altri obesi rivelavano che il cancro induceva un aumento della frequenza ASC nella circolazione sistemica di ben sei volte. Gli Autori ottenevano anche prove che le ASC mobilitate in questo modo potevano essere assunte nei tumori, incorporate nei vasi sanguigni come periciti, potendosi differenziare in adipociti in un modo dipendente dall’obesità. Estendendo questa prova, si scopriva che la vascolarizzazione maggiore del tumore, come risultato della variazione della morfologia e un aumento di due volte della densità, si associava con adipociti intratumorali e con la proliferazione elevata delle cellule maligne circostanti. Secondo gli Autori, l’insieme dei loro risultati suggeriva che le ASC reclutate dal tessuto adiposo endogeno potevano essere assunte dal tumore, potenziando le proprietà di sostegno del microambiente (Cancer Res., 72 (20); 5198-208. © 2012)
In conclusione, i risultati avrebbero indicato che l'obesità può accelerare la crescita del tumore indipendentemente dalla dieta concorrente. In effetti, di là dai molti processi sistemici attraverso i quali l'obesità può favorire il cancro, questo studio ha focalizzato il ruolo potenziale del WAT in eccesso. La prova di questo fenomeno è emersa, peraltro, in altri studi recenti degli Autori che hanno ipotizzato per il WAT, oltre alla funzione di secrezione delle adipochine, anche quella di servire come fonte di cellule reclutate dal tumore e stimolanti lo stesso attraverso la secrezione locale di fattori paracrini. Così che, i risultati di questo studio indicano che i progenitori mesenchimali assunti nei tumori, almeno in parte provengono dal WAT. Pur tuttavia, il midollo osseo rimane pur sempre la fonte autentica delle cellule ematopoietiche che contribuiscono al microambiente tumorale. I dati degli Autori suggeriscono, peraltro, che una combinazione di elevata disponibilità delle ASC e del loro traffico di segnalazione comporta nell'obesità l'incremento netto del loro reclutamento nei tumori. La mobilitazione delle ASC osservata nell’obesità, in concomitanza con il loro accumulo nello stroma / vascolarizzazione tumorali, indica che il WAT contribuisce al pool delle cellule mesenchimali del cancro. I dati dello studio sono contro la possibilità di una proliferazione significativa delle ASC infiltranti, come determinanti della loro abbondanza nei tumori. Inoltre, i dati suggeriscono che la CXCL1 (Chemokine (C-X-C motif) ligand 1) e l’IL-8 (interleukin – 8), secreta dalle cellule tumorali e la segnalazione tramite i recettori CXCR1 o CXCR2 (chemokine receptors) sono implicati nella migrazione delle ASC omentali umane.
I percorsi specifici molecolari attraverso i quali le ASC possono contribuire alla progressione del cancro sono ancora da stabilire. I dati di questo studio indicano, invero, che le ASC reclutate dai tumori diventano perivascolari o si differenziano in adipociti intratumorali. In precedenza era stato dimostrato che i progenitori mesenchimali, tra cui le ASC, modulavano la sopravvivenza cellulare, l'angiogenesi e la risposta immunitaria. Tale dato potrebbe spiegare i loro effetti di promozione del tumore. Riferimenti recenti in modelli murini indipendenti e in campioni clinici sugli adipociti tumorali sono in accordo con i risultati di questa ricerca. Inoltre, il non aver osservato in un recente studio un accumulo di lipidi nelle cellule maligne riportate avrebbe suggerito agli Autori che il metabolismo e i meccanismi di accumulo dei lipidi tumorali possono essere specifici per un tipo di cancro. I dati della maggiore copertura nell'obesità di periciti dei vasi tumorali suggerivano anche una pervietà vascolare aumentata con una conseguente maggiore sopravvivenza e proliferazione delle cellule maligne per effetto delle ASC. Peraltro, questa possibilità è coerente con gli effetti proangiogenici delle molecole secrete dalle ASC.
In sintesi, questo studio, come affermato dagli Autori, prevede il reclutamento nei tumori delle cellule derivate dal WAT come cooperatore potenziale degli effetti stimolatori dell'obesità sulla progressione della neoplasia. Tale dato solleverebbe una questione in merito alla sicurezza delle procedure di lipotransfer nei malati neoplastici tanto che i ricercatori hanno proposto le ASC come bersaglio potenziale di terapia.
J.Y. Petit dell’European Institute of Oncology, Milan – Italy e collaboratori, proprio riguardo all’ampia diffusione dell’innesto di grasso nella ricostruzione del seno delle pazienti con cancro, nel non chiaro ruolo del tessuto adiposo, hanno analizzato: cinquantanove pazienti con neoplasie intraepiteliali, sottoposte a lipofilling, senza recidiva tra chirurgia primaria e lipofilling e 118 pazienti abbinate come gruppo di controllo con i corrispondenti intervalli liberi da recidiva (Ann Oncol. 2013 Feb 7). L'endpoint primario con follow-up a partire dalla linea di base era costituito da un evento locale (LE). Il follow-up era di sessantatré e sessantasei mesi dall'intervento e trentotto e quarantadue rispetto al basale per i gruppi di lipofilling e di controllo rispettivamente. A cinque anni l'incidenza cumulativa di LE era del 18% e del 3% (P = 0.02). Nelle analisi di sopravvivenza univariata l’indice di proliferazione Ki-67 era il fattore significativo. Un'analisi per sottogruppi mostrava che il lipofilling aumentava il rischio di LE nelle donne con meno cinquanta anni, con alto grado di neoplasia, Ki-67 maggiore o uguale a quattordici o che avevano subito una quadrantectomia.
In conclusione, il rischio maggiore di LE si osservava nelle pazienti con neoplasia intraepiteliale dopo lipofilling per cui gli Autori, anche riconoscendo la necessità di ulteriori studi di conferma, suggerivano l’opportunità d’informazione in tali casi.
Hursting SD della Case Western Reserve University, Cleveland – USA hanno, per loro conto, richiamato l’attenzione sui diversi fattori correlati all'obesità che possono influenzare la comparsa di un tumore, la sua progressione e / o la risposta alla terapia (Cancer Prev Res (Phila). 2012; 5(11):1260-72). Gli Autori hanno, quindi, riproposto il ruolo chiave di questi fattori dell'ospite sugli effetti complessi del rapporto obesità e cancro e suoi esiti. Essi comprendono, invero, l’insulina, l’insulin-like growth factor-I, la leptina, l’adiponectina, gli ormoni steroidei, le citochine e le molecole legate all'infiammazione. Ognuno di essi è considerato nel contesto del bilancio energetico e come potenziale bersaglio per la prevenzione del cancro. La possibilità di prevenzione a livello dei sistemi deve, quindi, comprendere la restrizione energetica, la composizione della dieta e l’esercizio fisico.
Vucenik I e Stains JP del Duke University School of Medicine, Durham, USA, proprio riferendosi al crescente problema di salute in tutto il mondo rappresentato dall’obesità spesso associata alla sindrome metabolica, diabete, malattie cardiovascolari, ipertensione e altre patologie croniche, quali anche diversi tipi di cancro, tra cui quello del colon, della mammella, dell’endometrio, del fegato, dei reni, dell’esofago, dello stomaco, del pancreas, della cistifellea e anche la leucemia, hanno ribadito l’interesse scientifico di chiarire i meccanismi biologici alla base delle relazione tra queste malattie (Ann N Y Acad Sci. 2012; 1271:37-43).
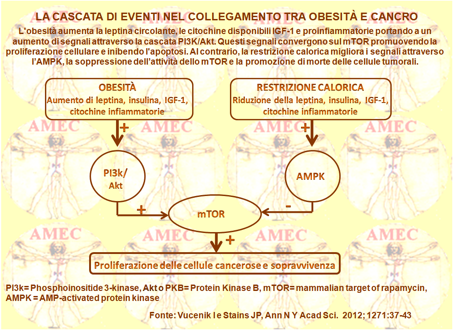
Essi, in effetti, comprendono la modulazione del bilancio energetico, la restrizione calorica, i fattori di crescita, le molteplici vie di trasmissione dei segnali e dei processi infiammatori. Essenziale tra le vie di segnalazione che collegano l'obesità e il cancro è la cascata PI3K/Akt/mTOR, che rappresenta un obiettivo dei diversi fattori associati all'obesità e che regola la proliferazione e la sopravvivenza cellulare. La comprensione dei meccanismi molecolari e cellulari che intervengono nella connessione tra l’obesità e il cancro costituisce, peraltro, la condizione importante per lo sviluppo delle terapie potenziali. Comunque, il legame convince a ripetere la raccomandazione di mantenere un peso corporeo sano per tutta la vita, come una delle strategie più importanti per proteggersi contro le neoplasie maligne.
Il cancro nell’accezione comune
L'oncologo R.A. Willis definì in patologia, in forma poi accettata a livello internazionale, il termine tumore, derivato dal latino tumor, come l’equivalente di rigonfiamento. Usò anche la denominazione di neoplasia, dal greco νεοπλασία, per definire una nuova formazione o una massa anormale di tessuto che cresceva in eccesso e in modo disordinato, persistendo in questo stato dopo la cessazione degli stimoli che ne avevano indotto la formazione. In seguito, si è appurato che la crescita abnorme di un gruppo di cellule a scapito dell'omeostasi tissutale è determinata dalle alterazioni del loro patrimonio genetico ed è alla base di una vasta classe di malattie classificate in rapporto alle loro diverse caratteristiche, ma principalmente in tre modi:
- secondo il tipo istologico originario delle cellule proliferanti, principalmente nel caso dei tumori epiteliali, mesenchimali, delle cellule del sangue o del tessuto nervoso,
- secondo l'aggressività e il decorso clinico previsto, in tumori benigni, non cancerosi, e in maligni, cancerosi o cancro,
- secondo la stadiazione tumorale, o classificazione TNM, per quanto riguarda i tumori maligni.
Le neoplasie maligne sono comunemente chiamate cancro. Esse hanno la caratteristica di invadere e distruggere i tessuti circostanti e possono diffondersi a distanza dalla loro sede di origine, producendo metastasi e, infine, provocare la morte dell'ospite.
Con neoplasia secondaria si definisce, invece, qualsiasi tumore che rappresenta una forma metastatica di un tumore primario.
Il sistema TNM, come definito dall’AJCC (American Joint Committee on Cancer ), è il sistema di stadiazione più comunemente usato e si basa su tre parametri: profondità dell’infiltrazione neoplastica (T), grado di coinvolgimento dei linfonodi regionali (N) e presenza dei siti di malattia a distanza (M). Il parametro T può variare da 1 a 4 in rapporto alla sua dimensione da più piccola a più grande, potendo essere "is" ovvero "in situ". Il T4 solitamente non esprime solo la grandezza, ma anche l'infiltrazione di organi vitali limitrofi. Il parametro N esprime la condizione dei linfonodi in rapporto con il tumore, variando dallo stato indenne di “0” sino alla gravità crescente di “3”. Il parametro M è riferito alle metastasi a distanza, variando da “0” per loro assenza o di “1” per la loro presenza. Si adotta una descrizione con una "x" a termine in caso di mancata nozione dell'esatta estensione a distanza della malattia, indicando che sono necessari ulteriori esami di approfondimento.
Il termine “G” esprime il grado di aggressività del tumore o di differenziazione cellulare della neoplasia e può estendersi da “1” a “4”.
Il peso globale del cancro
Le stime contemporanee dell'incidenza di mortalità, prevalenza e DALY (disability-adjusted life years) dei principali tipi di tumori a livello nazionale per 184 paesi del mondo del progetto GLOBOCAN della WHO per il 2008, pubblicate da Ahmedin Jemal dell’American Cancer Society, Atlanta, GA e collaboratori, hanno riportato globalmente circa 12.700.000 nuovi casi di tumore con 7,6 milioni di morti per cancro e 28,8 milioni di sopravvissuti nel giro di cinque anni dalla diagnosi. Il cancro ai polmoni è rimasto il più comune al mondo (CA Cancer J Clin 2011;61:69–90). Difatti, con i suoi 1.6 milioni di nuovi casi è al primo posto delle neoplasie maligne con il 12,7% del totale. Con gli 1,4 milioni di decessi ha contribuito al 18,2% della mortalità totale. Al secondo posto segue il cancro al seno femminile con 1,4 milioni di casi e il 10,9% dei totali, ma al quinto posto nei termini di causa di decesso con 458.000 morti, pari al 6,1%. I tumori del colon e del retto con 1,2 milioni di malati e 608.000 morti, quello dello stomaco con 990.000 e 738 mila, della prostata con 913.000 e 261 000 e del fegato con 748.000 e 695.000 rispettivamente si pongono progressivamente dal terzo al sesto posto nei termini di frequenza globale di nuovi casi. Pur tuttavia, il più comune rispetto alla prevalenza è stato il cancro al seno femminile con 5,2 milioni di donne che sopravvivono fino a cinque anni dopo la diagnosi, seguito da quello del colon-retto con 3,3 milioni e della prostata con 3,2 milioni di uomini.
Previsioni in Europa della mortalità per cancro
M. Malvezzi dell’Istituto di Ricerche Farmacologiche “Mario Negri” di Milano e collaboratori, considerando l’importanza delle stime attuali di mortalità del cancro per definire le priorità della prevenzione e del trattamento, utilizzando i modelli di conteggio logaritmico di Poisson sulla mortalità, hanno valutato il numero di decessi e i tassi standardizzati per età nel 2012 di tutti i tumori di cancro e delle sedi selezionate per l'intera Unione europea (UE) e per i sei paesi più densi di popolazione (Ann Oncol. 2012 Apr;23(4):1044-52). I dati sono stati quelli riferiti al periodo 1970-2007 e fino l’anno più recente disponibile per la Francia (2007), la Germania (2006), l’Italia (2007), la Polonia (2008), la Spagna (2008) e il Regno Unito (2009).
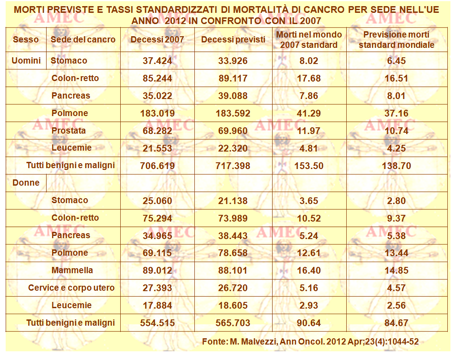
Le morti per cancro nel 2012 erano stimate pari a 1.283.101, 717.398 per gli uomini e 565.703 per le donne, corrispondenti ai tassi complessivi di morte per cancro standardizzati di 139/100 000 uomini e 85/100 000 donne. Il calo rispetto al 2007 era uguale al 10% per gli uomini e al 7% per le donne. Negli uomini la riduzione prevista per lo stomaco era -20%, per le leucemie -11%, per il polmone e la prostata -10% e per il colon-retto -7%. Nelle donne i valori erano corrispondentemente -23% per lo stomaco, - 12% per le leucemie, -11% per l’utero e il colon-retto e -9% per la mammella. Quasi stabili del 2-3% erano i tassi attesi per il cancro del pancreas, mentre vi era un aumento del +7% per il cancro al polmone femminile. Le donne più giovani dell'unione europea e di tutti i singoli paesi, ad eccezione della Polonia, mostravano le maggiori cadute dei tassi di mortalità per cancro al seno con il -17%.
Sempre Malvezzi M e collaboratori con la stessa metodologia e popolazione hanno stimato il numero di morti e l’ASR (age-standardized (world) mortality rates) nel 2013 per tutti i tipi e selezionati tumori (Ann Oncol. 2013 Mar;24(3):792-800). Il numero previsto di decessi per il 2013 per il cancro nell'Unione europea è risultato di 1.314.296, di cui 737.747 uomini e 576.489 donne. Tra il 2009 e il 2013 tutte le ASR per cancro prevedono un calo del 6% a 140.1/100.000 uomini, e del 4% a 85.3/100 000 donne. Le ASR per 100.000 comprendono 6,6 uomini e 2,9 donne per lo stomaco e rispettivamente 16,7 e 9,5 per l’intestino, 8.0 e 5,5 per il pancreas, 37,1 e 13,9 per il polmone, 4.2 e 2.6 per la leucemia, 10,5 per la prostata negli uomini, 14,6 per il seno nelle donne e 4.7 per il cancro uterino. Le recenti tendenze appaiono favorevoli, tranne che per il cancro del pancreas e del polmone nelle donne.
In conclusione il trend favorevole continuerà anche nel 2013. Da notare che il tumore al pancreas è divenuto la quarta causa di morte per cancro in entrambi i sessi, mentre in pochi anni il cancro del polmone diventerà probabilmente la prima causa di mortalità per cancro nelle donne sorpassando, così, anche il cancro al seno.
Recenti dati epidemiologici delle neoplasie maligne in Italia
I recenti dati, diffusi da epicentro dell’Istituto Superiore di Sanità sulla base del rapporto AIRTUM 2012, riportano per l’Italia circa 364.000 nuovi casi di cancro con un’incidenza del 56% nei maschi e del 44% nelle femmine. Tali dati epidemiologici escludono, però, le neoplasie maligne della cute, stimati nell’ordine di circa 67.000. Il cancro del colon-retto con gli oltre 50.000 nuovi casi è stato il più frequente, seguito da quello della mammella con 46.000, del polmone con 38.000 e della prostata con 36.000. Il cancro del polmone ha rappresentato, però, la prima causa di morte oncologica per gli uomini, mentre per le donne lo è stata quello della mammella. I dati dell’ISTAT riportano, peraltro, che in Italia nel 2009 i tumori hanno contribuito a 174.678 decessi, il 29,7% dei 588.438 totali, subito dopo i 224.830, corrispondenti al 38,2%, delle malattie del sistema circolatorio. Pur tuttavia, da una parte nelle donne le malattie cardiovascolari sono state la prima causa di morte con i 127.060 decessi pari al 42,1% del totale e i tumori la seconda con i 76.112 decessi pari al 25,2%. Dall’altra, la prima causa di morte negli uomini è stata rappresentata, invece, dai tumori con 98.566 decessi, pari al 34,4%, seguiti dalle malattie del sistema cardiocircolatorio con 97.770, pari al 34,1%. Comunque, come risultato incoraggiante, i dati hanno indicato che la sopravvivenza dei malati oncologici a cinque anni era aumentata rispetto al passato. In particolare, secondo il rapporto AIRTUM 2011 – Sopravvivenza (Epidemiologia & Prevenzione 2011; 35 (5-6) Suppl. 3), in Italia la sopravvivenza dei malati di tumore è continuata ad aumentare con la differenza di 4-10 punti percentuali in meno al Sud rispetto al Centro-Nord. Più precisamente la sopravvivenza dei malati oncologici, con esclusione di quelli della vescica e della cute, a cinque anni dalla diagnosi è stata pari al 50% per gli uomini e al 60% per le donne, dato superiore alla media europea e simile a quello dei Paesi scandinavi. Essa, peraltro, è arrivata al 94% nel cancro della tiroide, all’87% in quello della mammella della donna, all’89% in quello della prostata, al 61% in quello della cervice uterina e al 58% in quello del colon-retto. Mentre per le leucemie è stata del 43%, del 29% per il cancro dello stomaco, del 14% per quello del fegato e del 13% per quello del polmone.
Milena Sant della Fondazione IRCSS Istituto Nazionale dei Tumori, Milano, Italy e collaboratori, basandosi sulla possibilità di trovare i motivi della forte variazione geografica nella sopravvivenza del cancro in tutta Italia dagli studi dei modelli di cura del registro dei tumori della popolazione, hanno fornito una panoramica della cura erogata ai malati italiani di cancro (Cancer Epidemiology Vol. 36, 6, 541-547, Dec. 2012). Gli Autori hanno, quindi, selezionato da quattordici registri dei tumori italiani campioni a caso di pazienti adulti con melanoma della pelle, cancro del seno, del colon e del polmone non a piccole cellule, diagnosticati nel periodo 2003-2005. Lo stadio di diagnosi al seno, al colon e di melanoma era più precoce al nord / Italia centrale, rispetto ai registri meridionali. Gli Odds Ratio di cure standard erano inferiori a quelli di riferimento a Sassari (0,68, 95% IC 0,51-0,90) e a Napoli (0,48, 95% IC 0,35-0,67) per il tumore al seno, non differivano tra i registri per il cancro del colon Dukes C; erano più elevati in Romagna (3,77, 95% IC 1,67-8,50) e più bassi a Biella (0,38, 95% IC 0,18-0,82) per il tumore del polmone. Per il melanoma erano più alti a Reggio Emilia (2,37, 95% IC 1,12-5,02) e inferiori a Ragusa (0,27, 95% IC 0,14-0,54).
In conclusione, nonostante le limitazioni dovute alle variazioni della disponibilità delle informazioni cliniche e delle differenze nella fase di distribuzione dei registri tra il nord / centro e il sud, lo studio, secondo gli Autori, avrebbe dimostrato la persistenza d’importanti disparità nella cura del cancro in tutta Italia, peraltro non riducibili in un immediato futuro.
Flessione dei tassi di morte per il cancro
Ahmedin Jemal del Surveillance Research Program, American Cancer Society, Atlanta e collaboratori hanno di recente riportato che i tassi generali di morte per il cancro del polmone, del colon-retto, del seno femminile e della prostata hanno mostrato una flessione negli Stati Uniti, coinvolgendo in questa tendenza favorevole entrambi i sessi e tutti i principali gruppi razziali ed etnici (JNCI J Natl Cancer Inst Vol. 105, Issue 3, Feb. 2013.). Al contrario, per quanto riguarda i tumori del fegato, del pancreas, dell'utero e il melanoma soltanto negli uomini i tassi di mortalità hanno continuato ad aumentare, come pure per altri tumori, come alcuni associati all’infezione da HPV in ragione della probabile bassa copertura vaccinale.
Secondo gli Autori, i fattori che avrebbero contribuito ai risultati epidemiologici favorevoli nei riguardi del cancro del polmone, del colon-retto, della mammella femminile e della prostata dovevano, di certo, ricondursi alla riduzione dei fattori di rischio importanti, come il fumo, e al miglioramento della diagnosi precoce e del trattamento, come lo screening di massa e la chemioterapia adiuvante. I motivi, invece, da considerare per i tassi di mortalità crescenti in entrambi i sessi per i tumori del pancreas e del fegato e negli uomini per il melanoma e nelle donne per il cancro dell'utero dovevano ancora essere chiariti. Tuttavia, queste tendenze avrebbero dovuto, almeno in parte, giustificarsi: con l’elevata prevalenza dell'infezione cronica da virus epatite C per il cancro del fegato; con l’aumento della prevalenza dell'obesità per il fegato, il pancreas e l'utero; con l’aumento dell'esposizione alle radiazioni dannose ultraviolette per il melanoma. Peraltro, per tutti questi quattro tipi di cancro si erano rilevati corrispondenti aumenti dei loro tassi d’incidenza. Inoltre, anche per tumori supplementari, come quelli della tiroide e del rene, si era osservato un trend crescente d’incidenza, probabilmente almeno in parte per le maggiori possibilità di diagnosi legate alla più ampia applicazione delle tecniche d’imaging, ma anche per l’aumento dell’obesità.
In definitiva, nonostante i progressi sostanziali nella prevenzione del cancro e nell’adozione dei mezzi di controllo, come avvenuto per molti tumori come quello del polmone, del colon-retto, del seno femminile e della prostata, l'incidenza e / o i tassi di mortalità sono stati osservati in aumento per alcune sedi come il fegato, il pancreas, il rene, la tiroide e il melanoma. Tale dato indicherebbe per gli Autori la necessità di ulteriori ricerche eziologiche con l'identificazione dei principali fattori di rischio per lo sviluppo degli interventi più appropriati con i programmi e le strategie di provata efficacia, favorendo il più ampio accesso alla diagnosi e al trattamento precoce.
In effetti, negli USA si muore di meno per colpa del cancro. Tra il 2000 e il 2009 la mortalità è scesa di circa il 2% negli uomini e dell’1,5% nelle donne. Nei bambini sotto i quattordici anni, poi, è diminuita quasi del 2%. A stabilirlo è stato il rapporto annuale sull’incidenza dei tumori negli Stati Uniti, elaborato dal National Cancer Institute e dai Centers for Disease Control di Atlanta e pubblicato dalla rivista 'Journal of the National Cancer Institute'. Questi dati che si riferiscono agli Stati Uniti, afferma Umberto Tirelli direttore del dipartimento di oncologia medica dell'Istituto Tumori di Aviano, si potrebbero facilmente trasferire alla situazione in Italia. Negli uomini il calo della mortalità riguarda soprattutto i tumori del polmone, della prostata, del colon e dello stomaco, mentre nelle donne il cancro della mammella, della cervice, dell’ovaio, della vescica e del polmone.
Tale dato di fatto, ha affermato lo scienziato italiano, suggerisce la necessità di combattere più efficacemente il fumo e di ottenere un miglioramento sia nella diagnosi più precoce sia nei trattamenti più tempestivi ed efficaci. La sfida del futuro, secondo il ricercatore, è quella di migliorare i sistemi di lotta al Papilloma virus umano e all’obesità. Nei riguardi di quest’ultima è in crescita, invero, la prevalenza dei tumori associati, come quelli del rene, del pancreas, dell’utero e del fegato.
Evidenze sull’associazione tra obesità e cancro
Ament Z dell’Elsie Widdowson Laboratory UK e collaboratori hanno esaminato il ruolo che la metabolomica, tra cui la lipidomica, ha giocato nel chiarire l’azione dei PPAR (peroxisome proliferator-activated receptors) nella regolazione del metabolismo sistemico, così come negli aspetti del cancro farmaco-indotto e nel metabolismo xenobiotico (Genome Med. 2012; 4(4):32). Gli studi relativi hanno definito i ruoli dei PPARδ nel regolare l'ossidazione degli acidi grassi nel tessuto adiposo e l'interazione tra l’invecchiamento e il PPARα nel fegato. I potenziali vantaggi di questi approcci traslazionali riguardano l'ampliamento del ruolo degli agonisti dei PPAR e un migliore monitoraggio dell’efficacia dei farmaci. I PPAR, com’è noto, sono un insieme di tre recettori ormonali nucleari con un ruolo chiave nella regolazione del metabolismo, in particolare nel passaggio tra lo stato di sazietà e quello del digiuno e nelle vie metaboliche che coinvolgono l'ossidazione degli acidi grassi e il metabolismo dei lipidi. Inoltre, al di fuori del metabolismo, rivestono un certo numero d’importanti ruoli di controllo e di sviluppo. I PPAR sono anche i potenti obiettivi per il trattamento del diabete di tipo 2, della dislipidemia e dell’obesità. Tutto ciò anche se un certo numero dei singoli agonisti sia stato collegato a effetti collaterali indesiderati e vi sia una complessa relazione tra i PPAR e lo sviluppo del cancro.
Edward A. Lew e Lawrence Garfinkel dell’American Cancer Society, dopo un lungo periodo di studio prospettico condotto nel periodo 1959-1972, hanno descritto la mortalità in funzione delle variazioni di peso tra 750.000 uomini e donne della popolazione generale (J Chronic Dis 1979; 32: 563–576). I valori più bassi si riscontravano nelle persone vicine al peso medio e in quelle con il 10-20% sotto a esso. Nei casi con il 30-40% del peso maggiore la mortalità era di circa il 50% superiore rispetto a quelli del peso medio. Con oltre il 40% in più si toccava quasi il 90%. La mortalità per cancro era elevata solo tra coloro con il 40% o più di sovrappeso. Il cancro del colon e quello del retto erano, peraltro, le sedi principali per la mortalità degli uomini, mentre quelli della cistifellea e delle vie biliari, del seno, della cervice, dell’endometrio, dell’utero e delle ovaie lo erano per le donne. La malattia coronarica era, però, il fattore principale della mortalità più elevata nel sovrappeso, arrivando a essere superiore del 55% nei casi con il 30-40% in più del peso della media e del 100% circa tra coloro con oltre il 40% del sovrappeso. Inoltre, la mortalità per diabete era particolarmente elevata nel sovrappeso, soprattutto nelle donne. I risultati di questo studio epidemiologico di mortalità corrispondevano a quelli del Build and Blood Pressure Study del 1959, basati sull’esperienza delle assicurazioni.
Wendy Demark-Wahnefried dell’University of Alabama e collaboratori hanno, in effetti, ribadito il ruolo dei fattori di rischio per l'incidenza del cancro nell’obesità, come condizione determinata dallo squilibrio energetico, e dai livelli sub-ottimali dell’attività fisica (Cancer Epidemiol Biomarkers Prev August 2012 21; 1244-1259). Hanno anche riproposto l’evidenza della loro importanza anche dopo la diagnosi del cancro e la loro influenza sul decorso della malattia, così come sulla salute generale, sul benessere e sulla sopravvivenza. Gli Autori hanno, così, precisato che lo stile di vita e gli interventi medici, che di fatto li modificano, sarebbero alla base del controllo del cancro. La revisione eseguita dagli studiosi riassumeva, in effetti, gli argomenti di discussione principali che sono stati affrontati nel recente workshop dell’Istituto di Medicina dal titolo "The Role of Obesity in Cancer Survival and Recurrence". La discussione includeva: i meccanismi dell’influenza e della progressione del cancro associati con l'obesità e con il bilancio energetico, la complessità di studio e l'interpretazione del bilancio energetico sulla ricorrenza del cancro e alla sopravvivenza, le associazioni tra l’obesità e il rischio di cancro, la recidiva e la mortalità, gli interventi che favoriscono la perdita di peso, l’aumento dell'attività fisica, il bilancio energetico negativo come mezzo di controllo del cancro, le prospettive future.
La perdita di peso, invero, ha dimostrato di determinare una significativa riduzione del rischio delle diverse malattie correlate all’obesità, quali il diabete tipo 2 e le malattie cardiovascolari. Sulla traccia di tal evidenza si è anche ipotizzata una riduzione dell'incidenza di mortalità per i tumori correlati all’eccesso di peso. Diversi sono stati, quindi, i lavori pubblicati sulla valutazione di tale legame.
Wolin KY e Colditz GA della Washington University School of Medicine, St Louis nella loro revisione aggiornata ritrovavano evidenze dell’International Agency for Research on Cancer report del 2002 (Br J Cancer. 2008 Oct 7;99(7):995-9. Epub 2008 Aug 26). L'accento era posto sul decorso della malattia e sulle implicazioni per il controllo del peso per prevenire il cancro e portavano alla conclusione che la perdita di peso avrebbe potuto impedire una parte importante dei tumori più comuni, come il cancro del colon, quello al seno dopo la menopausa e quello della prostata. In seguito, gli studi più importanti sull’argomento hanno interessato condizioni dettate dalla chirurgia bariatrica, dimostrando l'utilità del ricorso a questa terapia.
Renehan AG dell’University of Manchester, UK e collaboratori hanno eseguito una revisione sistematica e una meta-analisi per valutare la forza dell’associazione tra la BMI e i diversi tipi di cancro e per indagare le differenze di queste associazioni tra i sessi e i gruppi etnici (Lancet. 2008 Feb 16;371(9612):569-78). A seguito di ricerche elettroniche dal 1966 al novembre 2007, hanno identificato studi prospettici di venti tipi di cancro. Hanno, quindi, fatto una metanalisi casuale sugli effetti e una metaregressione delle stime incrementali specifiche dello studio per determinare il rischio di cancro associato con un aumento di 5 kg/m2 della BMI. Erano, così, analizzati 221 set di dati, pari a 141 articoli, tra cui 282.137 casi incidenti. Negli uomini a ogni aumento di 5 kg/m2 della BMI si associava fortemente l’adenocarcinoma esofageo (RR 1.52, p <0.0001), della tiroide (1.33, p = 0.02), del colon (1,24, p <0,0001) e del rene (1,24, p <0,0001). Nelle donne si registravano forti associazioni tra un aumento di 5 kg/m2 della BMI e il cancro dell'endometrio (1.59, p <0.0001), della colecisti (1.59, p = 0.04), dell’esofago (1.51, p <0.0001) e del rene (1,34, p <0,0001). Si notavano associazioni positive più deboli (RR <1.20) negli uomini tra il maggiore indice di massa corporea e il cancro rettale e il melanoma maligno. Nelle donne le stesse deboli correlazioni si registravano, invece, con il cancro della mammella in post-menopausa, del pancreas, della tiroide e del colon. In entrambi i sessi erano in causa la leucemia, il mieloma multiplo e il linfoma non-Hodgkin.
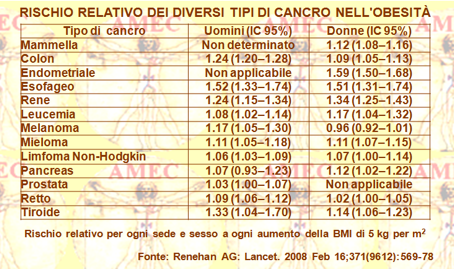
Per il cancro del colon le associazioni erano più forti di due punti negli uomini, rispetto alle donne (p <0,0001). Inoltre, le correlazioni erano generalmente simili negli studi dell’America settentrionale, Europa, Australia e le regioni Asiatiche del Pacifico. In quest’ultima area del mondo, peraltro, si registravano forti correlazioni tra la BMI e i tumori al seno in premenopausa (p = 0,009) e postmenopausa (p = 0,06).
In conclusione, sulla base del loro studio, gli Autori affermavano che l’aumento della BMI si associava a un aumentato rischio dei tumori maligni più comuni e meno comuni. Inoltre, per alcuni tipi di cancro, le correlazioni differivano tra i sessi e le popolazioni delle diverse origini etniche, tanto da suggerire ulteriori esplorazioni sui meccanismi biologici di questo legame.
S. Birks della Monash University Melbourne, Victoria, Australia e collaboratori hanno compiuto una recente recensione con il proposito di esaminare la letteratura riguardante l’effetto di tutti i tipi di perdita di peso sull’incidenza del cancro e sulla mortalità e di descrivere in modo più chiaro il rapporto tra questi due fattori (Obesity Reviews Volume 13, Issue 10, pages 868–891, October 2012). Hanno, così, identificato trentaquattro studi osservazionali, tranne uno, per la maggior parte riportanti pesi auto-riferiti e senza la definizione dell’intenzionalità della perdita di peso. Peraltro, sedici dei trentaquattro lavori avevano trovato una significativa associazione inversa tra la perdita di peso e l'incidenza del cancro o della mortalità. Per il resto, i risultati erano stati nulli. L'associazione osservata era stata più coerente in cinque dei sei studi con indagine dell'effetto della perdita di peso intenzionale. Peraltro, la riduzione del rischio era stata maggiore per i tumori correlati all'obesità e nelle donne.
In conclusione, secondo i risultati acquisiti, gli Autori dichiaravano che la perdita di peso intenzionale si era tradotta in una minore incidenza di cancro, in particolare quello femminile e correlato all’obesità. Tuttavia, affermavano la necessità di ulteriori valutazioni con maggiore attenzione per le popolazioni maschili.
Oggi si stima da più parti che circa il 40% dei casi di cancro dell'endometrio, il 25% dei casi di quello renale e il 10% di quello al seno e del colon potrebbero essere evitati mantenendo un indice di massa corporea (BMI) inferiore ai 25 kg per m2.
Peraltro, il Workshop Summary del 3 aprile 2012 dell’IOM (Istitute of Medicine), The Role of Obesity in Cancer Survival and Recurrenc, riportava che le recenti ricerche suggeriscono che l'eccesso di peso e l'obesità possono influenzare la sopravvivenza del cancro e le recidive. D’altro canto, il crescente tasso dell’obesità e dell'invecchiamento della popolazione rende le popolazioni sempre più suscettibili al cancro, alimentando la sempre più diffusa preoccupazione per il ruolo dell'obesità nella crescita del tumore. C’è, quindi, grande interesse a esplorare sempre più nuovi ed efficaci modi per rompere il legame tra queste due malattie, specialmente in presenza già di un tumore, perché vi sarebbe maggiore suscettibilità alla progressione maligna o alla sua recidiva o alla sua presentazione in altra sede.
Tarabra E del Presidio Sanitario Gradenigo Torino e collaboratori hanno considerato come il cancro del colon-retto (CRC) rappresenti un problema sanitario importante in Italia, essendo la seconda causa di morte per cancro dopo di quello polmonare negli uomini e quello al seno nelle donne (Eur J Intern Med. 2012; 23(1):65-9). Hanno voluto, così, compiere uno studio per meglio chiarire i meccanismi alla base del ruolo dell’obesità nel CRC tenendo conto del recente SNP (polimorfismo a singolo nucleotide) del gene FTO (fat mass and obesity associated), risultato significativamente associato con l'obesità. In particolare, gli Autori hanno teso a stabilire se lo SNP rs9939609 FTO potesse rappresentare nella popolazione italiana un fattore di rischio per il CRC e l’adenoma. Hanno, così, arruolato 1.037 soggetti suddividendoli in tre gruppi:
1) 341 pazienti con CRC, M / F = 197/144, età media = 65,17 ± 11,16 anni,
2) 385 pazienti con adenoma del colon-retto, M / F. = 247/138, età media = 62,49 ± 13,01 anni,
3) 311 controlli sani, M / F = 150/161, età media = 57,31 ± 13,84 anni.
Il DNA è stato estratto dal sangue intero e conservato congelato per la genotipizzazione rs9939609 mediante real-time PCR.
La frequenza dell’obesità associata all’allele A mutato (AA + AT) sul gene FTO era 69,77% tra i controlli e 71,85% e 65,71% rispettivamente tra i CRC e i pazienti con polipo. Rispetto ai soggetti di controllo il genotipo dell’AA + AT non aveva effetti significativi sul rischio sia per i CRC (OR = 1,106, IC 95% = 0,788-1,550, p = 0,561) sia per gli adenomi colorettali (OR = 0,830, IC 95% = 0,602-1,144, p = 0.255). Non si osservava alcuna associazione tra il genotipo AA e la localizzazione CRC / polipo e l'età al momento della diagnosi. Come misurato in un gruppo di pazienti, i portatori degli alleli di rischio non riflettevano una BMI significativamente alterata.
In conclusione le varianti FTO legate all’obesità nella popolazione italiana non avrebbero svolto, secondo gli Autori, un ruolo importante nel modulare il rischio di cancro del colon-retto.
Yang WH della National Yang-Ming University, Taipei Taiwan e collaboratori hanno descritto come la RAC 1 medi la migrazione delle cellule del cancro indotto dall’attivazione della Twist 1 (Nat Cell Biol. 2012 Mar 11;14(4):366-74). L’EMT (Epithelial-mesenchymal transition), caratterizzata dalla soppressione della proteina di adesione E-caderina, è un processo fondamentale per la promozione delle metastasi e delle proprietà similstaminali delle cellule tumorali. Tuttavia, la dissociazione degli aggregati cellulari non sarebbe sufficiente a spiegare lo spostamento delle cellule tumorali e, quindi, sfugge ancor oggi la natura della mobilità delle cellule tumorali sottoposti all’EMT. Gli Autori hanno, così, identificato un meccanismo con cui si stimola il movimento delle cellule cancerogene mediante l'attivazione del RAC 1. La Twist 1 coopera con la BMI1 nel sopprimere l’espressione della let-7i. Si ottiene, così, la sovraregolazione dello NEDD9 e del DOCK3, l’attivazione del RAC 1, consentendo la modalità del movimento mesenchimale tridimensionale. In effetti, nella clinica dei pazienti con cancro della testa e del collo l'attivazione dell'asse Twist 1 - let-7i - NEDD9 si correla con l'invasività e il peggiore risultato del tumore.
Parekh N della New York University, USA e collaboratori, considerando che il ruolo dell'obesità sulla sopravvivenza del cancro è poco conosciuto pur essendo un noto fattore di rischio, hanno condotto una revisione sistematica della letteratura per valutare l'evidenza sulla prognosi del tumore della prostata, del colon-retto e della mammella, tre delle più comuni sedi colpite dall'adiposità (Annu Rev Nutr. 2012; 32:311-42). Gli Autori hanno, così, esaminato trentatré studi di cancro al seno, sei di quello alla prostata e otto del colon-retto. Le evidenze erano riferite abbondantemente alla sopravvivenza del cancro alla mammella, mentre erano scarse nei meriti del cancro della prostata e del colon-retto. Nel complesso, però, la maggior parte studi sosteneva una relazione tra l’adiposità e la mortalità o la progressione del cancro specifico per sede. Tuttavia, secondo gli Autori, la maggior parte delle ricerche non era stata specificamente progettata per studiare questi risultati e, di conseguenza, si sarebbero dovute considerare diverse questioni metodologiche prima di integrare i dati ottenuti e trarne le conclusioni.
Green DM dello St Jude Children's Research Hospital, Memphis – USA e collaboratori hanno dovuto costatare che molti partecipanti del CCSS (Childhood Cancer Survivor Study) erano ad aumentato rischio di obesità per causa probabilmente multifattoriale, ma non ben compresa (J Clin Oncol. 2012; 30(3):246-55). Hanno, così, voluto valutare il potenziale contributo dei fattori demografici, di stile di vita, di trattamento, intrapersonali e dell’uso farmaceutico auto riferito per l’obesità con indice di massa corporea ≥ 30 kg/m2 in 9.284 adulti maggiori di diciotto anni, partecipanti al CCSS. Hanno anche identificato i predittivi indipendenti utilizzando modelli di regressione multivariabile. Le correlazioni sono state determinate con SEM (structural equation modeling). I fattori di rischio indipendenti per l'obesità includevano il cancro diagnosticato da cinque a nove anni di età (rischio relativo [RR], 1,12, 95% IC, 1,01-1,24, p = .03), l’alterazione della funzione fisica Short Form-36 (RR, 1,19, 95% IC, 1,06-1,33; uso P < .001), le radiazioni ipotalamo / ipofisi a dosi da venti a trenta Gy (RR, 1.17, 95% IC, 1,05-1,30 p = .01) e l’uso della paroxetina (RR 1.29, 95% IC, 1,08-1,54, p = .01). Le linee guida dell’incontro dell’US Centers for Disease Control and Prevention per l’intensa attività fisica (RR, 0,90, 95% IC, 0,82-0,97, p = .01) e per una quantità media di ansia (RR, 0,86, 95% IC, da 0,75 a 0,99; P = .04) riducevano il rischio dell’obesità. I risultati della SEM (n = 8.244; indice misura comparativa = 0,999; indice di Tucker Lewis = 0,999; radice dell'errore quadratico medio di approssimazione = 0,014; radice quadrata del residuo medio ponderato = 0,749) descrivevano, peraltro, l'impatto gerarchico dei predittivi diretti, moderatori e mediatori dell'obesità.
In conclusione, secondo gli Autori il trattamento, lo stile di vita e i fattori intrapersonali, così come l'uso degli antidepressivi specifici, potevano contribuire all'insorgenza dell’obesità tra i sopravvissuti, mentre un intervento poliedrico, tra farmaco alternativo e altre terapie per la depressione e l'ansia, avrebbe potuto ridurne il rischio.

