NOTIZIARIO Novembre 2014 N°10
PRINCIPI INNOVATIVI DI RAPPORTARSI
CON IL CANCRO
A cura di:
Giuseppe Di Lascio §
Con la collaborazione di:
Cancro non più inguaribile e soprattutto prevenibile
Proprio a riguardo di quanto enunciato, torna utile annotare che Francesco Cognetti, oncologo e presidente della fondazione “Insieme contro il cancro”, in occasione della presentazione al ministero della Salute del suo libro in un convegno nazionale giovedì 24 luglio 2014 a Roma, “Il male (in)curabile. I progressi nella lotta contro il cancro e il nuovo ruolo della comunicazione”, ha affermato che oggi giorno si guarisce in oltre il 50% dei casi senza sensazionalismi della malattia.
In particolare, al momento attuale le percentuali di guarigione più elevate si riscontrano con il 91% negli uomini con carcinoma alla prostata, con lo 87% nelle donne con cancro al seno e con il 64% e il 63% negli uomini e nelle donne rispettivamente con cancro del colon-retto. Di recente quindi, per cambiare l'approccio culturale alla malattia e anche per migliorare la consapevolezza dei cittadini rispetto all'importanza e all'efficacia della prevenzione, gli esperti hanno sfidato i media, ammonendoli a non parlare più di male incurabile.
Nel 1970, in effetti, la quota delle percentuali di guarigione della malattia raggiungeva a mala pena il 30 per cento. Nota ancora dolente era, però, il dato dell’aumento esponenziale della sua incidenza a causa del costante invecchiamento della popolazione e del progresso nella diagnosi. Peraltro, per questi stessi motivi le proiezioni del 2020 stimano per l’Italia una quota di 4,5 milioni di casi di tumore, contro i tre del 2013.
Si rendono, quindi, indispensabili un’attenta e oculata prevenzione ed anche una diffusa e corretta informazione a tutti i livelli.
Si è anche valutato che il possibile risparmio dei costi sanitari, che potrebbe essere realizzato nel nostro Paese con le efficaci campagne di prevenzione oncologica, dovrebbe corrispondere in cinque anni a sei miliardi di euro. La cifra, peraltro, con l’estensione delle iniziative a tutti gli Stati membri dell’Europa raggiungerebbe i ben cinquanta miliardi complessivi. In effetti, il costo totale del cancro nel nostro continente ammonta annualmente a 126 miliardi di euro, mentre in Italia è di soli sedici circa. Da notare che nel 2012 le nuove diagnosi di cancro sono state in Europa 3.450.000 con 1.750.000 morti, pari a tre decessi il minuto. Il tumore più costoso si è dimostrato, con i 18.8 miliardi annuali, quello al polmone, seguito da quello al seno con i 15,0, da quello al colon-retto con i 13.1 e da quello alla prostata con gli 8.43. La spesa media europea per la cura di ogni paziente affetto da cancro si è dimostrata pari a 102 euro, con forti variabilità nazionali. Difatti, in Bulgaria è stimata pari a sedici euro, in Polonia a trentasette, in Romania a venti, in Portogallo a cinquantatré, in Gran Bretagna a ottantacinque, in Spagna a novantaquattro, in Francia a centodieci, in Italia a centoquattordici e in Germania a centottantadue.
In conformità a tutto quanto riportato, conviene sempre ribadire che le principali istituzioni e associazioni scientifiche che si occupano di oncologia, tra cui l’AIOM (Associazione Italiana di Oncologia Medica), sono concordi nell’affermare che circa il 40% dei tumori è potenzialmente prevenibile modificando lo stile di vita. In particolare, tale indicazione riveste una certa importanza per i tumori degli organi maggiormente sensibili, quali quello del colon-retto, dello stomaco, della prostata, della mammella, dei polmoni e della pelle.
Le principali misure da adottare sono:
- Abolire il fumo anche passivo, che causa il 25-30% di tutti i tumori. Ogni anno nel mondo si contano tre milioni di decessi per l’uso del tabacco, che riduce mediamente l’aspettativa di vita di otto anni.
- Moderare il consumo di alcol, che aumenta il rischio di cancro del cavo orale, della faringe, dell’esofago e della laringe. Inoltre, in entrambi i sessi si associa anche fortemente all’insorgenza del cancro al fegato e all’intestino e nelle donne a quello della mammella.
- Adottare una dieta a base di frutta e verdure, come quella mediterranea, per il dimostrato forte effetto protettivo contro numerose forme tumorali, in particolare dell’apparato digerente e respiratorio. In effetti, l’alto contenuto in fibre e in vitamine favorisce l’attività antiossidante e la maggior motilità intestinale, che riduce l’assorbimento delle sostanze cancerogene.
- Evitare l’eccesso ponderale e l’obesità. È dimostrato, difatti, che il sovrappeso, uguale o superiore al 40%, determina un rischio più elevato di mortalità per cancro del colon-retto, della prostata, dell’utero, della cistifellea e della mammella. In particolare, gli studi epidemiologici hanno rilevato la correlazione tra i grassi di origine animale e il rischio dei tumori e delle malattie cardiovascolari. L'obesità, in effetti, come principale causa evitabile di cancro, sta sorpassando rapidamente il tabacco.
- Evitare la sedentarietà e praticare attività fisica. I sedentari, difatti, presentano il 20-40% di probabilità maggiori di ammalarsi. Al contrario, l’attività fisica praticata ha un effetto protettivo sin dalla giovane età e dura nel tempo.
- Proteggersi dai raggi solari ed evitare lampade solari facendo attenzione ai nèi e ai noduli cutanei.
- Fare attenzione alle malattie sessualmente trasmissibili, considerando che il 15-20% dei tumori deriva da infezioni che possono essere prevenute.
- Evitare l’uso delle sostanze dopanti. Difatti, gli steroidi anabolizzanti aumentano il rischio dei tumori, in particolare di quelli del fegato, della prostata e dei reni. Peraltro, le probabilità aumentano con gli anni di assunzione. Il GH/IGF1, ormone della crescita, può essere causa del linfoma e del cancro al seno, al colon e alla prostata. Le eritropoietine, invece, possono causare disordini ematologici.
La prevenzione come strategia essenziale nella lotta contro il cancro
Da qualche tempo, ormai, le organizzazioni di tutto il mondo preposte alla lotta contro il cancro promuovono campagne per sensibilizzare l'opinione pubblica e per portare i crescenti problemi del cancro all’attenzione del pubblico, dei capi di governo, dei politici e dei professionisti della salute.
In particolare, l’UICC (Union for International Cancer Control) e le organizzazioni partner hanno ribadito il valore della prevenzione contro il cancro nelle loro varie iniziative, tra cui la più importante quella annuale del World Cancer Day in cui l'intero mondo si unisce nella lotta a questa temibile malattia. Quest’azione rappresenta, invero, un’urgente strategia di vitale importanza per il suo enorme impatto sulla sofferenza umana, tenuto in debito contro che si prevede quasi il raddoppiamento entro il 2030 del numero dei malati globali nel mondo sino ai 21,4 milioni e con quasi i due terzi nei paesi a basso e medio reddito.
La convinzione dell'Organizzazione Mondiale della Sanità è, comunque, quella di poter ridurre del 25% entro il 2025 le morti da malattie non trasmissibili, come il cancro. Tutto ciò, però, è considerato possibile solo se si ottiene una convergenza delle forze per la realizzazione degli interventi. Il cancro, in effetti, non conosce confini, per cui tutti gli interessati devono assumersi la responsabilità di combatterlo.
È, comunque, incoraggiante e avvincente il fatto che nella giornata mondiale contro il cancro del 4 febbraio 2012, il tema principale sia stato: "Il cancro può essere prevenuto."
L’AICR (American Institute for Cancer Research) ha colto l'occasione per sottolineare che circa un terzo dei tumori più comuni può essere prevenuto modificando le abitudini di vita, come il mangiare sano, l’essere fisicamente attivi e il mantenersi di peso regolare. Tutto ciò, soprattutto, per le persone anziane, giacché il cancro diventa più comune con l’avanzare dell'età, senza essere, però, inevitabile. In definitiva, i piccoli cambiamenti salutari di uso quotidiano, che possiamo introdurre nel nostro comportamento di oggi, hanno, di certo, il valore per incidere positivamente sul minor numero di tumori del domani.
Pertanto, è bene rispondere urgentemente al quesito:
Che cosa fare per ridurre il proprio rischio per il cancro?
L’European Code Against Cancer ha tracciato proprio recentemente dodici suggerimenti per ridurre il rischio di cancro. Il tabacco occupa il primo posto della lista, seguito dal peso corporeo, dalla limitazione dell’esposizione al sole e dall’uso dell’alcol.
Il codice è stato redatto dallo IARC, agenzia dell'Organizzazione mondiale della sanità specializzata nella lotta contro il cancro, con la partecipazione della Commissione europea.

La relazione è una sintesi delle prove scientifiche, mentre il codice è in linguaggio quotidiano con utili indicazioni ai cittadini del mondo.
Per le donne in età fertile si precisa anche che l'allattamento al seno dovrebbe essere incoraggiato, perché riduce il rischio di cancro della madre. Per le donne in postmenopausa, invece, si ribadisce che la terapia ormonale sostitutiva dovrebbe essere limitata, perché aumenta il rischio di alcuni tumori, come quello della mammella, dell'endometrio e dell'ovaio. Per le ragazze si propone, peraltro, la raccomandazione della vaccinazione contro l’HPV (human papillomavirus) per prevenire il cancro del collo dell'utero e quella contro l'epatite B per i neonati per prevenire il cancro del fegato.
Riguardo a tutto ciò, sono essenziali i programmi di screening organizzati, come quelli per il cancro del colon-retto in entrambi gli uomini e le donne e per il seno e lo screening del cancro del collo uterino nelle donne.
Pur tuttavia, lo stile di vita salutare con mantenimento del peso normale del corpo e con un’attività fisica regolare è sempre certamente alla base per la riduzione il rischio del cancro.
Pronto il Pnp (Piano nazionale di prevenzione) 2014-2018
Per quanto riportato in precedenza è utile sapere che Il PNP (Piano nazionale della prevenzione), finora utilizzato con Intesa tra il Ministero della salute, le Regioni e le Province Autonome, si è caratterizzato per:
- la scelta strategica delle Regioni nel dichiarare di voler investire ulteriormente nell’area della prevenzione per raggiungere i maggiori risultati di salute,
- la decisione di mettere alla prova una linea di governance compartecipata, per cui il Ministero ha teso alla valorizzazione al meglio delle potenzialità del CCM (coordinamento del Centro per il controllo delle malattie), delle Regioni per innestare proficuamente nella loro pianificazione una serie di linee operative comuni e delle Aziende sanitarie – a cascata – per utilizzare tale strumento aggiuntivo e contribuire a ridurre in concreto il peso delle malattie e della disabilità.
- la decisione di subordinare la programmazione alle conoscenze disponibili.
In coerenza con la visione della salute, riconosciuta e condivisa a livello mondiale, il Piano nazionale di prevenzione tende a raccogliere la sfida dell’intersettorialità, investendo non solo nelle aree tradizionali della prevenzione, universale, selettiva, secondaria, ma anche promuovendo la salute. In questo modo, s’implementano quei processi orientati non a prevenire una o un limitato numero di condizioni patologiche, ma a creare nella comunità e nei suoi membri un livello di competenza con lo sviluppo dell’empowerment, necessario per il controllo delle malattie.
Il PNP 2014-2018, di recente stesura, ricalca questi principi, adottando percorsi condivisi. Questa strategia metodologica tende, così, a migliorare in tutti i livelli operativi coinvolti la qualità della programmazione, la comparabilità dei prodotti e dei risultati e la crescita culturale e delle competenze.
Gli obiettivi principali di questo Piano si possono così riferire:
- Limitare il carico delle malattie, riducendo gli eventi morbosi e mortali prevenibili e consolidando, in modo sempre più sostenibile anche in rapporto all’invecchiamento demografico, il benessere della popolazione.
- Investire sul benessere dei giovani, classe attiva, lavorativa e dirigente del futuro, la quale necessita di una crescita responsabile e consapevole con il seguire stili di vita sani e principi, contrari a qualunque forma di dipendenza, ma di ricerca di un benessere psicofisico e affettivo.
- Rafforzare e confermare il patrimonio comune delle pratiche preventive, come quelle a tutela della salute dei lavoratori e quelle della prevenzione oncologica e delle vaccinazioni.
- Rafforzare l’attenzione verso i gruppi fragili, tendendo a ridurre le diseguaglianze e prevenendo la disabilità.
- Considerare l’ambiente insieme all’individuo e alle popolazioni, promuovendo azioni rivolte sempre alla riduzione delle malattie, soprattutto croniche e non trasmissibili.
La versione finale del Pnp 2014-2018, che ha tenuto conto delle osservazioni delle Regioni, dovrà essere adottata con una delibera ad hoc dalle Regioni entro il 31 dicembre 2014. In seguito ed entro il 31 gennaio 2015, un Accordo Stato Regioni ne specificherà i criteri per la stesura, la valutazione e la certificazione.
Peraltro, per l’Intesa sottoscritta nel 2005, oltre alle risorse per la realizzazione degli obiettivi del Piano sanitario nazionale, anch’esse già previste dalla legge, sono disponibili 200 milioni di euro già destinati alla sua attuazione.
Le nuove linee guida NICE per i malati di cancro
Il National Institute for Health and Care Excellence dell’UK ha pubblicato le nuove e aggiornate raccomandazioni del novembre 2014 per i medici delle cure primarie riguardo al riconoscimento, alla gestione e alla richiesta di consulenza specialistica nel sospetto di cancro in età pediatrica, nei giovani e negli adulti. Le linee guida sono, in effetti, raccomandazioni per la cura di persone con specifiche condizioni o circostanze cliniche che comprendono la prevenzione, la cura sia attraverso l'assistenza primaria e sia quella secondaria con partecipazione anche dei servizi più specializzati. Esse, come ribadito nella stesura, si sono basate sulle migliori evidenze di efficacia clinica e di costo disponibili e sono state prodotte per aiutare professionisti e pazienti nelle scelte più informate e adeguate.
Si è riportato anche che il cancro è una condizione importante, sia in termini di numero di persone colpite e sia di grave impatto sul malato e su quanti gli sono vicino. Nel Regno Unito si diagnosticano circa 350.000 nuovi casi ogni anno, relativi a oltre 200 diversi tipi di cancro, che presentano individualmente diverse caratteristiche e possibili sovrapposizioni. Si precisa che circa un terzo della popolazione è portato a sviluppare la malattia nel corso della vita. La diagnosi precoce e i nuovi farmaci hanno permesso grandi progressi nel trattamento e consequenzialmente nella sopravvivenza.
Il medico di cure primarie deve riconoscere tempestivamente i sintomi, i segni e i risultati anomali dei test. Le raccomandazioni, quindi, elencano le caratteristiche per offrire le informazioni chiave ai professionisti sulle particolari modalità di comparsa e di associazione dei tumori a un dato insieme di sintomi, segni o risultati d’indagini.
È posta evidenza per: una distensione addominale, una massa pelvica o un aumento di volume di un organo, un dolore pelvico, un riflesso assente, un’anemia con o senza mancanza di ferro, una massa anale, un’anoressia o una perdita di appetito o una sazietà precoce, un nodulo ascellare, un mal di schiena, un’ematemesi, un’ematuria, un’emottisi, un sanguinamento genitale o rettale o comunque inspiegabile, un dolore o un rigonfiamento osseo, un nodulo al seno, dei lividi o delle petecchie, delle alterazioni delle funzioni neurologiche centrali, una linfoadenopatia cervicale, un cambiamento delle abitudini intestinali, un’infezione o un dolore toracico, un ippocratismo delle dita, una tosse, dei sintomi cutanei, una trombosi venosa profonda, un’insorgenza di diabete, una diarrea, una dispepsia, una disfagia, una dispnea, una disuria, una disfunzione erettile, una stanchezza, un sangue occulto nelle feci, una febbre, una frattura, un’epatomegalia o un’epatosplenomegalia, una raucedine, una linfoadenopatia inguinale, un ittero, un qualsiasi nodulo o massa, una qualsiasi linfoadenopatia, una sudorazione notturna, una modifica dei capezzoli, una lesione orale, un pallore, delle condizioni che riguardano i genitori, un prurito, una mancanza di respiro, dei sintomi testicolari e/o penieni, una perdita di peso.
È riportata anche, per le informazioni e il sostegno dei pazienti, una serie di raccomandazioni, focalizzate su come rassicurarli circa il loro rischio di cancro con spiegazioni sugli eventuali trattamenti.
Esempi per cui le nuove linee guida raccomandano alla consulenza urgente di uno specialista sono:
- cambiamenti inspiegabili delle abitudini intestinali all’età di sessanta anni e oltre,
- inspiegabile sanguinamento rettale all’età di cinquanta anni e oltre,
- ittero all’età di quaranta anni e oltre,
- nodulo al seno inspiegabile con o senza dolore nelle donne di età di trenta anni e oltre,
- sanguinamento in postmenopausa nelle donne di età di cinquantacinque anni e oltre.
Seguire le regole dello stile di vita sano riduce il rischio e la mortalità per cancro
Ormai tutte le organizzazioni sanitarie e scientifiche raccomandano stili di vita sani per ridurre il rischio e la mortalità complessiva di cancro. Cynthia A. Thomson dell’University of Arizona e collaboratori, non avendo rilevato nei meriti una valutazione tra adesione ai comportamenti di salute di prevenzione del cancro e conseguente rischio della malattia in un campione eterogeneo di donne in postmenopausa, hanno voluto esaminarla per il punteggio dell’American Cancer Society (ACS) Nutrition and Physical Activity Cancer Prevention Guidelines e per il rischio di cancro, per la mortalità cancro-specifica e di tutte le cause in 65.838 donne in postmenopausa fra i cinquanta e i settantanove anni iscritte nel Women's Health Initiative Observational Study tra il 1993 e il 1998 in quaranta centri statunitensi (Cancer Prev Res; 7 (1) January 2014).
I punteggi da zero a otto punti delle linee guida ACS erano determinati da una misura combinata di dieta, di attività fisica, d’indice di massa corporea (correnti e all'età di diciotto anni) e del consumo di alcol.
Dopo un periodo medio di follow-up di 12,6 anni, erano individuati 8.632 tumori e 2.356 decessi per la malattia. I più alti punteggi delle linee guida ACS, rispetto ai più bassi, erano associati con un rischio inferiore del 17% di qualsiasi tipo di cancro [HR, 0.83; intervallo di confidenza (IC) 95% = 0,75-, 92]. Erano, inoltre, associati a un rischio inferiore del 22% di cancro al seno (HR, 0.78; IC 95%= 0,67-0,92), del 52% di cancro del colon-retto (HR, 0.48; IC 95%= 0,32-0,73), del 27% del rischio di mortalità per qualsiasi causa e del 20% del rischio di mortalità cancro-specifica (HR, 0,80; IC 95%= 0,71-0,90). Le associazioni con la minore incidenza e con la mortalità del cancro erano generalmente più forti tra le donne asiatiche, di colore e ispaniche, mentre più deboli tra i bianchi non-ispanici.
In conclusione, i comportamenti in armonia con le Nutrition and Physical Activity Cancer Prevention Guidelines erano associati nelle donne in postmenopausa con un minor rischio totale di cancro della mammella e del colon-retto e con una più bassa mortalità cancro-specifica.
Impatto dello stile di vita sano sul cancro del colon-retto
Secondo gli ultimi dati del GLOBOCAN 2012 il cancro colorettale (CRC) in tutto il mondo è il terzo tumore più comune negli uomini con il 10,0% del totale d'incidenza e 746.000 casi l'anno e il secondo nelle donne con il 9,2% e 614.000. A tale riguardo si rileva, però, un'ampia variazione geografica con quasi il 55% dei casi nelle regioni più sviluppate del mondo. La corrispondenza tra i tassi di frequenza del cancro e il livello di occidentalizzazione indica in modo coerente e legittimo il ruolo importante dello stile di vita tra i fattori eziologici della malattia. Il WCRF / AICR (World Cancer Research Fund/American Institute for Cancer Research), sostenendo questa ipotesi, hanno, in effetti, riconosciuto che l’alta attività fisica e il copioso apporto di fibra alimentare, di pesce, di frutta secca, di latticini e di frutta e verdura fresca si associano con un basso rischio di CRC, mentre l’alto indice di massa corporea (BMI) e della circonferenza della vita, il fumo, il consumo di alcol, e l’assunzione di carni rosse e lavorate sono legati a un più alto rischio.
A tale proposito, Krasimira Aleksandrova del German Institute of Human Nutrition Potsdam-Rehbrücke, Nuthetal, Germany e collaboratori hanno inteso sviluppare un HLI (healthy lifestyle index) composto di cinque fattori di stile di vita potenzialmente modificabili e corrispondenti a: peso sano, attività fisica, non fumo, limitazione del consumo di alcol, dieta salutare (BMC Medicine 2014 12:168).
Hanno anche voluto esplorare l’associazione di questo indice con l’incidenza del CRC, utilizzando i dati raccolti all'interno della coorte dell’EPIC (European Prospective Investigation into Cancer and Nutrition).
Quest’obiettivo traeva spunto dalla considerazione che, mentre i ruoli individuali di questi fattori di stile di vita erano stati ampiamente studiati, poco gli Autori rilevavano in letteratura sui loro effetti congiunti. Difatti, la maggior parte degli studi epidemiologici aveva esplorato i comportamenti individuali di salute, trattando gli altri fattori di stile di vita come covariate nei modelli statistici. Non si era tenuto conto, in effetti, che nella vita reale è raro che le persone pratichino comportamenti isolati. L’approccio multidimensionale sullo stile di vita, invece, dovrebbe offrire maggiori informazioni sull’eziologia della malattia con risultati più efficaci per la programmazione delle strategie di prevenzione. Inoltre, bisogna tenere conto delle differenze di associazioni con diversi fattori di stile di vita tra i diversi sottotipi anatomici del cancro del colon e del retto e della diversità di sesso. Ad esempio, questi rilievi sono stati già stati dimostrati per l'eccesso del peso corporeo, della circonferenza vita e per l’inattività fisica.
Dal 1992 al 2000 un totale di 347.237 uomini e donne dai venticinque ai settanta anni della coorte EPIC forniva al basale informazioni sulla dieta e sullo stile di vita. Nel corso di un follow-up medio di dodici anni, s’identificavano 3.759 casi di CRC. L'associazione tra un HLI e il rischio di CRC era valutata utilizzando modelli di rischio proporzionale di regressione di Cox e calcolando i PAR (population attributable risks).
Tenuto conto dei centri di studio, dell'età, del sesso e del grado d’istruzione, a fronte di zero o di un fattore di stile di vita sano, l'hazard ratio (HR) per il CRC era 0.87 (intervallo di confidenza95% (IC): 0,44-0,77) per due fattori, 0,79 (IC95%: 0,70-0,89) per tre, 0.66 (IC 95%: 0,58-0,75) per quattro e 0,63 (IC 95%: 0,54-0,74) per cinque. Il P era <0,0001. Le associazioni erano presenti sia per il tumore del colon e sia per quello del retto con HR, 0.61 (IC 95%: 0,50-0,74; P <0.0001) per il primo e 0.68 (IC 95%: 0,53-0,88; P <0,0001) per secondo (P-differenza per sottotipo di cancro = 0.10). Complessivamente, il 16% dei nuovi casi di CRC (il 22% negli uomini e l’11% nelle donne) era attribuibile alla mancanza di adesione a una combinazione di tutti e cinque gli stili di vita sani inclusi nell'indice.
In conclusione, gli stili di vita combinati (peso sano, attività fisica, non fumo, limitazione del consumo di alcol, dieta salutare) erano associati a una minore incidenza di CRC nelle popolazioni europee, caratterizzate da comportamenti di tipo occidentale.
Fitness cardiorespiratorio e mortalità per cancro
Negli ultimi decenni si è moltiplicato l'interesse sul rapporto bilancio energetico e cancro e si sono accumulate le evidenze a dimostrazione di un ruolo importante giocato dal dispendio calorico nella prevenzione della temibile malattia, sia nei riguardi della sua incidenza e sia della mortalità. A tale riguardo è bene precisare che i termini di attività fisica e di fitness cardiorespiratorio sono a volte usati in modo intercambiabile e che la loro correlazione può essere percepita elevata, mentre in realtà essa è modesta. Per attività fisica si considera qualsiasi movimento corporeo prodotto dalla contrazione del muscolo scheletrico che migliora la spesa energetica. In confronto, la forma fisica non indica alcun comportamento, ma raffigura piuttosto la capacità di raggiungere un certo standard di prestazioni o di condizione. Le indagini epidemiologiche hanno, invero, fermato l'attenzione sull’associazione tra attività fisica e cancro, mentre meno è stato studiato per il fitness cardiorespiratorio. I dati disponibili suggeriscono, però, un effetto benefico apparente del fitness cardiorespiratorio sulla mortalità per tumore.
In effetti, studi meccanicistici hanno dimostrato che l'impatto positivo del fitness cardiorespiratorio coinvolge percorsi biologici che influenzano la sensibilità all'insulina, l'infiammazione cronica, i livelli degli ormoni steroidei, la produzione del fattore di crescita, l'immunità innata, la capacità antiossidante, la riparazione del DNA, la proliferazione cellulare e l'apoptosi.
A tal proposito, è bene ripetere che, per il raggiungimento di almeno un livello moderato di fitness cardiorespiratorio, bisogna seguire un’attività aerobica di moderata intensità per un minimo di 150 minuti o di settantacinque a settimana, se vigorosa. Peraltro, poiché l'attività fisica dimostra un rapporto dose/risposta inversa con il rischio delle malattie croniche e della mortalità, si raggiungono ulteriori vantaggi se si è in grado di superare questi limiti.
D. Schmid e M. e F. Leitzmann dell’University of Regensburg, Germany hanno condotto una revisione sistematica e una metanalisi sull’associazione tra fitness cardiorespiratorio e mortalità totale per cancro (Ann Oncol. 2014 Jul 9. pii: mdu250).
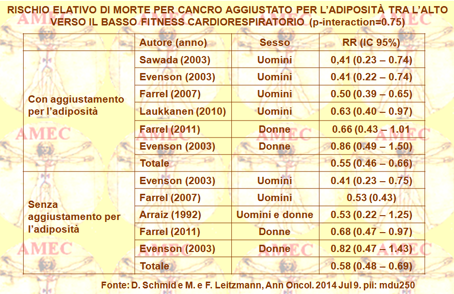
Gli Autori hanno, così, identificato in modo indipendente rilevanti studi nella letteratura scientifica fino all’agosto 2013, ottenendo le stime del rischio di sintesi con l’uso dei modelli degli effetti casuali.
Includevano, quindi, sei studi prospettici con un follow-up medio di 16,4 anni per un numero complessivo di 71.654 persone e 2.002 casi di mortalità totale per cancro. Il fitness cardiorespiratorio mostrava una forte, graduale associazione inversa con la mortalità totale per cancro. Utilizzando il basso fitness cardiorespiratorio, come gruppo di riferimento, i suoi livelli intermedi ed elevati correlavano statisticamente in modo significativo con la diminuzione dei rischi relativi (RR) di sintesi della mortalità per cancro totale, rispettivamente di 0,80 (intervallo di confidenza (IC) 95%= 0,67-0,97) e di 0,55 (IC 95% = 0,47-0,65). I dati regolati per l'adiposità producevano risultati simili.
In conclusione, l’aumento del fitness cardiorespiratorio rappresentava un forte predittivo di diminuzione del rischio totale di mortalità per tumore, indipendentemente dall’adiposità.
Sedentarietà e cancro
L’aumento smodato dell’uso negli ultimi anni della televisione e del computer, soprattutto nelle persone con ridotto impegno fisico lavorativo, ha portato all’estrema conseguenza della vita sedentaria nella routine quotidiana. Alcune indagini demoscopiche indicano oggettivamente che gli adulti occupano dal 50 al 60% della loro giornata con comportamenti sedentari. Tutto ciò avviene in numerosi ambiti della vita, comprese le attività ricreative, come la visualizzazione della TV o comunque di video, l'uso del computer, la lettura, l’occupazione da seduti a una scrivania, l’uso di mezzi di trasporto, sedendo in un autobus, in auto, o in treno, e in manifestazioni delle attività sociali, come giocando alle carte.
Questo comportamento sedentario è ormai divenuto un potenziale fattore determinante di esiti deleteri per la salute ed è studiato da qualche tempo insistentemente per quantificare il suo ruolo dannoso nell’insorgenza di numerose malattie croniche. In effetti, il tempo prolungato, speso da seduti, riduce la spesa energetica conducendo inevitabilmente all’aumento del peso corporeo nel tempo. Inoltre, per quanto riguarda l’uso della televisione, si è dimostrato un concomitante aumento del consumo di alimenti malsani, come bevande zuccherate, dolci e comunque cibi ad alto tenore calorico, ricchi di grassi insaturi. Tale abitudine, inoltre, è correlata a una maggiore consuetudine al fumo. Com’è ormai noto, sia il fumo e sia l’obesità sono condizioni associate a un aumentato rischio di cancro, a differenza dell’attività fisica che, invece, lo riduce.
Sino a oggi, diversi studi epidemiologici hanno esaminato il comportamento sedentario riguardo all’incidenza del cancro, compresi i tumori del seno, del colon-retto, dell’endometrio, delle ovaie, del polmone, della prostata, dello stomaco, dell'esofago, dei testicoli, dei reni e il linfoma non-Hodgkin. Molti di essi hanno rilevato un apparente effetto negativo sull'incidenza del cancro in rapporto al tempo prolungato della stazione da seduti.
Janet S. Hildebrand dell’American Cancer Society, Atlanta, Georgia e collaboratori, proprio sull’evidenza epidemiologica dell'associazione inversa tra attività fisica e cancro al seno, hanno svolto uno studio su 73.615 donne in postmenopausa dell'American Cancer Society Cancer Prevention Study II Nutrition Cohort (Cancer Epidemiol Biomarkers Prev October 2013 22; 1906). Gli Autori ritenevano non chiaro se le correlazioni si potessero mantenere con l’attività moderata, come il camminare, e se potessero esistere differenze per lo stato di recettorialità per gli estrogeni (ER), per l’indice di massa corporea (BMI, kg / m2), per l’aumento di peso negli adulti, o per l'uso di PMH (postmenopausal hormones). Non appariva abbastanza chiara anche la relazione tra il tempo trascorso da seduti e il cancro al seno.
Un totale di 4.760 donne riceveva la diagnosi di cancro al seno tra il 1992 e il 2009 e gli Autori utilizzavano la regressione di Cox per stimare i rischi relativi multivariati e aggiustati (RR) della malattia in rapporto al totale delle attività fisiche ricreative, di quelle a piedi, e il tempo libero da seduti. Si valutavano, quindi, le differenze delle associazioni per lo stato di ER, di BMI, di aumento di peso e dell'uso di PMH. Le donne più attive con attività fisica superiore a quarantadue MET-ora / settimana sperimentavano un rischio di cancro al seno inferiore del 25% rispetto a quelle al più basso grado di attività con zero sino a meno di sette ore MET / settimana (intervallo di confidenza [ (IC)95%: 0,63-0,89; P = 0,01)]. Il quarantasette per cento delle donne riferiva come loro unica attività ricreativa il cammino. Tra queste donne si osservava un rischio inferiore del 14% per periodi di cammino uguali o superiori alle sette ore / settimana, rispetto a quelli uguali o inferiori a tre ore / settimana (IC 95%: 0,75-0,98). Le associazioni non differivano dallo stato di ER, di BMI, dell’aumento di peso, o dell’'uso di PMH. Il tempo da seduti non si associava al rischio. Secondo gli Autori i loro risultati, dimostrando che l'attività fisica, anche moderata ma costante, aiutava a ridurre i rischi legati alle patologie gravi quali il cancro, potevano senz’altro essere di grande interesse per la salute pubblica. (Cancer Epidemiol Biomarkers Prev October 2013 22; 1906).
In maniera completa Daniela Schmid e Michael F. Leitzmann dell’University of Regensburg, Germany hanno eseguito una ricerca della letteratura sino al febbraio 2014, selezionando gli articoli che si riferivano al comportamento sedentario rispetto all’incidenza del cancro (JNCI J Natl Cancer Inst (2014) 106 (7): dju098).
Gli Autori si sono soffermati solo sugli studi osservazionali con criteri uniformi d’inclusione, poiché quelli randomizzati e controllati erano difficili da eseguire su quest’argomento.
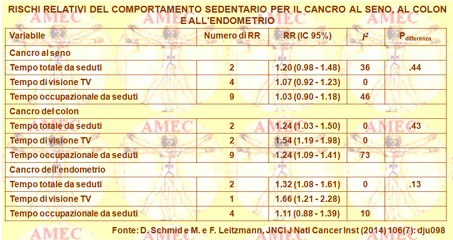
Erano, così, analizzati i dati di quarantatré studi osservazionali per un totale di 68.936 casi di cancro. Confrontando i livelli di tempo sedentario dal più alto vs il più basso, il rischio relativo (RR) per il tumore del colon era 1,54 (IC 95% = 1,19-1,98) per il tempo di visualizzazione della televisione, 1.24 (IC 95% = 1,09-1,41) per il tempo occupazionale da seduti e 1.24 (IC 95% = 1,03-1,50) per il tempo totale da seduti. Per il cancro dell'endometrio il relativo rischio era 1,66 (IC 95% = 1,21-2,28) per il tempo di visione della televisione e 1,32 (IC 95% = 1,08-1,61) per il tempo totale da seduti. Un’associazione positiva con il comportamento complessivo sedentario era nota anche per il cancro del polmone (RR = 1,21; IC 95% = 1,03-1,43). Il comportamento sedentario non era correlato, invece, al cancro del seno, del retto, delle ovaie, della prostata, dello stomaco, dell’esofago, dei testicoli, delle cellule renali e il linfoma non-Hodgkin.
In conclusione, la prolungata visione della televisione e il tempo trascorso in altre attività sedentarie erano associati a un aumentato rischio di alcuni tipi di cancro, specialmente per quello del colon e dell’endometrio, tumori notoriamente considerati correlati all’obesità. Al contrario, i rapporti tra il comportamento sedentario e il cancro al seno e del rene erano nulli, anche se l'obesità è spesso associata positivamente a tali neoplasie. Questo dato di fatto avrebbe suggerito agli Autori che il comportamento sedentario e l'obesità mediavano un rischio attraverso meccanismi comuni per alcuni tipi di cancro, come quello al colon-retto e all'endometrio. Per altri tipi di neoplasia, invece, come per il cancro al seno e il carcinoma renale si sarebbero dovuti riconoscere percorsi specifici e distinti dall’obesità.
Per loro conto Lynch BM dell’University of Melbourne, Australia e collaboratori hanno voluto studiare il comportamento sedentario (tempo trascorso da seduti) nello sviluppo del cancro alla prostata (Cancer Epidemiol Biomarkers Prev. 2014 May;23 (5):882-9).
Gli Autori hanno esaminato le potenziali associazioni del tempo giornaliero auto riferito passato nello stare seduto, guardando anche la televisione con il rischio di sviluppare o morire di cancro alla prostata tra 170.481 uomini del NIH-AARP Diet and Health Study. Gli Autori stimavano gli HR e gli intervalli di confidenza (IC) al 95% con il modello di rischio proporzionale di Cox. Tra il 1996 e il 2006, occorrevano 13.751 casi di cancro alla prostata, di cui 1.365 in fase avanzata. La mortalità fino al 2008 era di 669 casi. Nessuna forte e significativa associazione con il rischio di cancro alla prostata si osservava nei modelli corretti integralmente, sia per il tempo trascorso da seduti durante il giorno e sia passato davanti alla televisione o video. Vi erano alcuni effetti che suggerivano alcune interazioni con l’indice di massa corporea. L’aumento del rischio totale di cancro alla prostata si associava a un lieve, ma non significativo aumento del tempo di televisione / video tra gli uomini obesi (HR = 1.28; 95% IC: 0,98-1,69). Un’associazione nulla si osservava tra gli uomini in sovrappeso (HR = 1,04; 0,89-1,22), mentre per quelli con un BMI normale il tempo di televisione / video correlava con una diminuzione non significativa del rischio (HR = 0.82; 95% IC: 0,66-1,01). Modelli simili si osservavano nel cancro della prostata avanzato e nella mortalità per esso per una condizione totale giornaliera di stare seduti e un tempo televisione / video.
In conformità a questi risultati, gli Autori concludevano che il comportamento sedentario sembrava giocare un ruolo limitato nello sviluppo del cancro alla prostata, pur non potendo escludere l'impatto di errori di misura sui risultati.
La sopravvivenza dei malati di cancro
In linea con quanto riportato in precedenza, l’AIRTUM (Associazione Italiana Registri Tumori) ha riportato i dati riguardanti il 2013 riguardanti i tumori in Italia. Il cancro è ancora la seconda causa di morte nel nostro Paese con il 30% di tutti i decessi dopo le malattie cardiovascolari. Pur tuttavia, chi sopravvive a cinque anni dalla diagnosi ha per alcuni tumori, come quello del testicolo, del corpo dell'utero, il melanoma, i linfomi di Hodgkin e in misura minore quello del colon-retto, prospettive di sopravvivenza vicine a quelle della popolazione che non ha mai avuto una neoplasia. Negli ultimi anni sono complessivamente migliorate le percentuali di guarigione, per cui il 63% delle donne e il 55% degli uomini malati sono ancora vivi a cinque anni dalla diagnosi. In tutto ciò, va riconosciuto, soprattutto, il merito della maggiore sensibilità e adesione alle campagne di screening, con possibilità della diagnosi precoce e della maggiore efficacia delle terapie. Per l’appunto, difatti, se tutti adottassero gli stili di vita corretti e aderissero ai protocolli di screening, quasi il 70% dei tumori potrebbe essere prevenuto o diagnosticato in tempo.
In Italia i valori di sopravvivenza, sostanzialmente in linea con quelli dei Paesi nordeuropei, degli Stati Uniti e dell'Australia, sono aumentati nel corso del tempo e migliorano man mano che ci si allontana dal momento della diagnosi. È particolarmente elevata dopo cinque anni nei tumori più frequenti, come quello al seno con l’87% e quello alla prostata con il 91%.
Carol E. DeSantis dell’American Cancer Society, Atlanta e colleghi, proprio in considerazione del continuo aumento del numero dei sopravvissuti al cancro a causa dell'invecchiamento, della crescita della popolazione e del miglioramento della diagnosi precoce e del trattamento, hanno collaborato con l'American Cancer Society e il National Cancer Institute per una stima del numero dei sopravvissuti al cancro attuali e futuri, utilizzando i dati del SEER (Surveillance, Epidemiology, and End Results). Inoltre, in base alle informazioni contenute nella National Cancer Data Base, del SEER e del SEER-Medicare, hanno descritto i modelli di trattamento attuali per la maggior parte dei tipi di cancro più comuni. Il primo gennaio 2014 quasi 14,5 milioni di americani con una storia di cancro risultavano ancora in vita con previsione di una loro ascesa sino a quasi diciannove milioni entro il primo gennaio 2024. I tre tumori prevalenti più comuni tra i maschi erano quelli della prostata con il 43%, del colon-retto con il 9% e il melanoma con l’8%. Nelle femmine i più prevalenti erano, invece, i tumori maligni della mammella con il 41%, del corpo dell'utero con l’8% e del colon e del retto con l’8%. La distribuzione dei sopravvissuti per età variava notevolmente per tipo di tumore. Ad esempio, la maggior parte dei sopravvissuti al cancro della prostata nel 62% era di età compresa tra i settanta anni o più, mentre solo il 32% dei sopravvissuti per melanoma era in questo gruppo di età più avanzata. Gli Autori affermavano che queste informazioni costituivano per i medici un dato importante per capire i bisogni sanitari e psicosociali dei sopravvissuti al cancro e per valutare e gestire questi problemi in modo proattivo (CA CANCER J CLIN 2014; 00:00–00).
La sopravvivenza per i tumori ematologici in Europa
Dai primi anni 2000 si sono resi disponibili nuovi farmaci mirati al trattamento delle neoplasie ematologiche, tra cui gli anticorpi monoclonali anti-CD20 per il linfoma diffuso a grandi cellule B e la leucemia linfoblastica acuta, l’imatinib per la leucemia mieloide cronica e gli inibitori del proteasoma per il mieloma. Questi trattamenti hanno migliorato notevolmente la prognosi nella leucemia mieloide cronica, in molti tumori linfoidi e in misura minore nel mieloma multiplo. Tuttavia, questi vantaggi sono stati principalmente documentati in una serie di studi controllati o ospedalieri.
Milena Sant della Fondazione IRCCS Istituto Nazionale dei Tumori, Milan – Italy, utilizzando i dati dell’EUROCARE e dei raggruppamenti morfologici dell’HAEMACARE, hanno inteso stimare l'andamento nel tempo della sopravvivenza nella popolazione di undici neoplasie linfoidi e mieloidi in venti paesi europei, per regione e per età (The Lancet Oncology, Volume 15, Issue 9, Pages 931 - 942, August 2014).
Nel loro studio osservazionale retrospettivo, gli Autori includevano pazienti di età tra i quindici anni e oltre con diagnosi di neoplasia ematologica diagnosticata fino al 31 dicembre 2007 e seguita fino al 31 dicembre 2008. Si utilizzavano i dati di trenta registri dei tumori di venti paesi europei con informazione dell'incidenza continua e dei dati di buona qualità 1992-2007.
Per quattro periodi di tre anni (1997-99, 2000-02, 2003-05, 2006-08) gli Autori si servivano di un approccio ibrido per la stima per ogni malignità della sopravvivenza generale e standardizzata all’età e relativa a cinque anni di età specifiche per cinque regioni (UK, Europa del nord, del centro, del sud e dell’est). Per ogni malattia, stimavano anche per periodo, per età e per regione il relativo eccesso di rischio di morte per cinque anni dopo la diagnosi. Si analizzavano, quindi, 560.444 casi e dal 1997-99 al 2006-08 la sopravvivenza aumentava per la maggior parte dei tumori maligni. Il più cospicuo aumento si registrava per il linfoma diffuso a grandi cellule B dal 42·0% [IC 95%: 40·7-43·4] al 55·4% [54·6-56·2], p <0·0001. Per il linfoma follicolare si registravano valori dal 58·9% [57·3-60·6] al 74·3% [72·9-75·5], p <0·0001), per la leucemia mieloide cronica dal 32·3% [30·6-33·9] al 54·4% [52·5-56·2], p <0·0001) e per la leucemia promielocitica acuta, secondo stime non standardizzate per l’età, dal 50·1% [43·7-56·2] al 61·9% [57·4-0-66], p = 0·0038,). Altre variazioni in aumento della sopravvivenza si osservavano per il linfoma di Hodgkin dal 75·1% [74·1-76·0] a 79·3% [78·4-80·1], p <0·0001), per la leucemia linfocitica cronica / per il piccolo linfoma linfocitico dal 66·1% [65 · 1-67 · 1] al 69·0% [68·1-69·8], p <0·0001), per il mieloma multiplo / plasmocitoma dal 29·8% [29·0- 30·6] al 39·6% [38·8-40·3], p <0·0001), per la precursor lymphoblastic leukaemia/lymphoma dal 29·8% [27·7-32·0] al 41·1% [39·0-43·1], p <0·0001), per la leucemia mieloide acuta, esclusa la promielocitica acuta, dal 12·6% [11·9-13·3] al 14·8% [14·2-15·4], p <0·0001) e per altre neoplasie mieloproliferative, esclusa la leucemia mieloide cronica, dal 70·3% [68·7-71·8] al 74·9% [73·8-75·9], p <0·0001).
La sopravvivenza, leggermente aumentata nell’Europa meridionale, lo era di più nel Regno Unito e molto cospicuamente nel nord, nel centro e nell'Est del continente, ma in quest’ultima area in tono inferiore rispetto alle altre regioni. Inoltre, la sopravvivenza diminuiva con l'avanzare dell'età e aumentava con il tempo solo leggermente nei pazienti di settantacinque anni, anche se si verificava un aumento del 10% nei pazienti anziani con linfoma follicolare, in quello diffuso a grandi cellule B e nella leucemia mieloide cronica.
Queste tendenze erano incoraggianti e con molta probabilità legate all'impiego diffuso dei nuovi trattamenti, molto più efficaci di un tempo. Tuttavia, le differenze di sopravvivenza persistenti in Europa suggerivano anche variazioni nella qualità delle cure e nella disponibilità di questi nuovi trattamenti.
Valore dello screening tomografico per il cancro polmonare
Il cancro al polmone, il cui collegamento al fumo è ormai un dato accertato, rappresenta, invero, nel mondo la più grande causa di morte per neoplasia. A tale proposito, il NLST (National Lung Screening Trial) ha dimostrato che negli accaniti fumatori anziani la mortalità per questa malattia era di ben sette volte inferiore con l'uso di tre anni di annuale screening a basse dosi di tomografia computerizzata spirale che con l'uso della radiografia del torace. Inoltre, il PLCO (Prostate, Lung, Colorectal and Ovarian Cancer Screening Trial) ha anche riportato che, tra i circa 30.000 partecipanti con caratteristiche di base simili a quelle del NLST, la mortalità per il cancro ai polmoni non differiva in modo significativo tra chi era sottoposto a screening mediante la radiografia torace e quelli che ricevevano le cure tradizionali.
In linnea con quanto enunciato, Timothy R. Church dell’University of Minnesota e collaboratori hanno riportato lo screening, la diagnosi, i limitati risultati del trattamento della prima serie dei controlli del NLST (N Engl J Med 2013;368:1980-91)
Dall'agosto 2002 ad aprile 2004, gli Autori hanno, così, arruolato da trentatré centri degli Stati Uniti partecipanti asintomatici dai cinquantacinque ai settantaquattro anni di età con una storia di dedizione al fumo di almeno trenta pacchetti in un anno. I 53.439 iscritti erano assegnati in modo casuale a sottoporsi a screening annuale per tre anni e in particolare 26.715 con l'uso di una TC a basso dosaggio e 26.724 di radiografia del torace. I noduli o gli altri reperti sospetti erano classificati come risultati positivi. Il 98,5%, pari a 26.309 partecipanti del primo gruppo, e il 97,4%, pari a 26.035 del secondo, si sottoponevano allo screening e un totale di 7.191, pari al 27,3%, contro 2.387, pari al 9,2% rispettivamente, dimostravano un risultato positivo di screening. Inoltre, nei due gruppi 6.369, pari al 90,4%, e 2.176, pari al 92,7%, ricevevano almeno una procedura diagnostica di follow-up, tra cui imaging in 5.717 (81.1%) e in 2.010 (85,6%) e chirurgia in 297 (4,2%) e 121 (5,2%) rispettivamente. Il cancro al polmone era, comunque, diagnosticato in 292 partecipanti (1.1%) nel gruppo a basso dosaggio di CT, contro i 190 (0,7%) del gruppo con radiografia (fase I in 158 vs 70 partecipanti e stadio IIB-IV in 120 vs 112). La sensibilità e la specificità erano 93,8% e 73,4% per la TC a basso dosaggio e 73,5% e il 91,3% per la radiografia del torace, rispettivamente.
In conclusione, i risultati iniziali NLST dello screening erano già coerenti con la letteratura esistente nei riguardi della TC a basso dosaggio e la radiografia del torace, suggerendo una riduzione della mortalità per tumore del polmone nei centri di screening con personale esperto in TC del torace.
Per loro conto Black WC del Dartmouth-Hitchcock medical center di Lebanon, New Hampshire hanno esaminato il rapporto costo-efficacia dello screening con TC a basso dosaggio nel NLST (N Engl J Med. 2014 Nov 6;371 (19):1793-802).
Il NLST (National Lung Screening Trial), studio condotto su oltre 50.000 adulti asintomatici tra i cinquantacinque e i settantaquattro anni, aveva permesso di rilevare, come precedentemente riportato, una riduzione del 16% della mortalità per cancro polmonare e una riduzione del 6,7% della mortalità per tutte le cause. Gli Autori nella loro analisi stimavano gli anni di vita media e i QALY (quality-adjusted life-years), unità di misura che combina durata e qualità di vita, i costi per persona e gli ICERs (incremental cost-effectiveness ratios) per tre strategie alternative:
- non screening,
- screening con la radiografia,
- screening con TC a basso dosaggio.
Le stime di anni di vita si basavano sul numero delle morti osservate verificatesi durante il processo e sulla sopravvivenza prevista delle persone ancora in vita alla sua fine. Gli adeguamenti della qualità erano ricavati da un sottogruppo di partecipanti selezionati per completare i sondaggi della qualità della vita. I costi erano basati sui tassi di utilizzo e sui rimborsi sanitari. Gli Autori eseguivano anche analisi dei sottogruppi definiti in base all’età, al sesso, alla storia di abitudine al fumo e al rischio di cancro ai polmoni, compiendo analisi di sensitività sulla base delle diverse ipotesi.
Rispetto alla strategia del non screening, il programma di diagnosi precoce con TC a basso dosaggio costava un supplemento di 1.631 dollari a persona (intervallo di confidenza [IC]95%: 1.557 a 1.709) e forniva un ulteriore 0,0316 di anni di vita a persona (IC 95%: 0,0154-0,0478) e uno 0,0201 QALY per persona (IC 95%: 0088-,0314). Le ICER corrispondenti erano 52 mila dollari per anno di vita guadagnato (IC 95%= 34.000 a 106.000) e $ 81.000 per QALY guadagnato (IC 95%= 52.000 a 186.000). Tuttavia, gli ICER variavano ampiamente nei sottogruppi e nelle analisi di sensibilità.
In conclusione, gli Autori affermavano che il rapporto costo-efficacia migliore si rilevava nelle donne più che negli uomini e tra i gruppi a rischio di cancro al polmone più alto rispetto a quelli con il più basso. Peraltro, la diagnosi precoce permetteva risultati di costo-beneficio buoni anche nei fumatori correnti rispetto agli ex e negli adulti rispetto ai giovani. Tutto ciò era verosimilmente dovuto al rischio di cancro al polmone più alto nei fumatori e negli anziani. Negli uomini, in effetti, il costo per ogni QALY guadagnato era di 147.000 dollari, mentre nelle donne 46.000. Inoltre, nel gruppo di età dai cinquantacinque e cinquantanove anni ogni QALY corrispondeva a 152.000 dollari, dai sessanta ai sessantaquattro 48.000, dai sessantacinque e sessantanove 54.000 e dai settanta e i settantaquattro anni 117.000.
Negli adulti obesi con cancro opportuno il dosaggio chemioterapico appropriato
Le dosi ottimali dei farmaci chemioterapici o delle loro combinazioni si stabiliscono generalmente attraverso studi clinici randomizzati controllati. Nei pazienti adulti con cancro il dosaggio del farmaco è tradizionalmente basato sulla superficie approssimativa del corpo. Esistono, peraltro, prove convincenti che le riduzioni della dose standard e d’intensità possono compromettere la sopravvivenza libera da malattia e quella globale. Tutto ciò ha portato a considerare l’ottimale chemioterapia un indicatore della qualità di cura. Ciò nonostante, molti pazienti obesi e in sovrappeso continuano a ricevere dosi di chemioterapia limitata e studi di pratica clinica hanno dimostrato che le dosi fino al 40% dei pazienti obesi sono limitate e non basate sul peso corporeo reale. Inoltre, molti oncologi continuerebbero a utilizzare il peso corporeo ideale, limitando l’uso della superficie corporea. Inoltre, nei soggetti in sovrappeso e obesi con cancro è stata documentata una notevole incertezza dei medici sulla selezione ottimale della dose, rivelata dalla notevole variazione nel dosaggio della chemioterapia. Così che, in questi malati in crescita epidemica nel mondo la pratica di dosi limitanti finisce con influenzare negativamente la qualità delle cure e dei risultati. In effetti, la chemioterapia sistemica, senza un pieno dosaggio basato sul peso e con riduzioni inopportune, può anche spiegare in parte i tassi di mortalità per cancro significativamente più alti osservati nei soggetti in sovrappeso e obesi. Peraltro, secondo evidenze farmacocinetiche di efficacia e di tossicità, devono considerarsi infondate le preoccupazioni in merito al sovradosaggio basato sull'uso del peso corporeo effettivo nel paziente obeso con cancro.
Jennifer J. Griggs dell’University of Michigan e collaboratori, per fornire raccomandazioni per il dosaggio appropriato del chemioterapico citotossico per gli obesi adulti con cancro, hanno condotto una revisione sistematica della letteratura sugli studi coinvolti nei tumori della mammella, dell'ovaio, del colon e del polmone, elaborando delle utili linee guida (J Clin Oncol 30:1553-1561).
Gli studi di pratica clinica dimostravano, in effetti, che, secondo infondate preoccupazioni circa la tossicità o il sovradosaggio, fino al 40% dei pazienti obesi ricevevano dosi limitate della chemioterapia, non basate sul peso corporeo effettivo. Il gruppo di studiosi, pertanto, raccomandava dosi piene chemioterapiche, ponderate soprattutto in ragione dell'obiettivo di cura per l’assenza di evidenze di aumentata tossicità a breve o a lungo termine negli obesi. In effetti, la maggior parte dei dati indicava che la mielosoppressione era la stessa, o addirittura meno accentuata, tra gli obesi rispetto ai normopesi. Peraltro, gli Autori segnalavano che:
- I medici avrebbero dovuto rispondere a tutte le problematiche di tossicità correlate al trattamento nei pazienti obesi, in modo uguale ai normopesi.
- L'uso di un dosaggio fisso di chemioterapico era raramente giustificato, ma poteva considerarsi solo per alcuni agenti selezionati.
- Ulteriori ricerche di farmacocinetica e farmacogenetica erano opportune per guidare il dosaggio appropriato dei pazienti obesi con cancro.
La gestione del cancro in gravidanza
La diagnosi di cancro durante la gravidanza rappresenta, invero, un’evenienza drammatica per chiunque. Essa, peraltro, comporta una serie di preoccupazioni non solo per la donna, ma anche per la sicurezza del suo concepimento. Negli ultimi decenni, seppur questa complessa condizione patologica sia rimasta sempre rara, la sua incidenza è in aumento, contando circa un caso ogni 1.000 o 2.000 gestanti. Ciò è certamente dovuto alla maggiore età media delle gestanti, essendo il cancro più frequente con il crescere dell'età.
Questo dato, invero, deve anche considerarsi una delle cause dell’incapacità degli ultimi anni, dimostrata sia dai medici e sia dalle donne, nell’affrontare questa particolare problematicità. Importante, peraltro a tale riguardo, è riaffermare che il cancro raramente colpisce il feto direttamente e che, quindi, una donna incinta portatrice della malattia può partorire un neonato sano. Difatti, solo alcuni tipi di cancro possono diffondersi alla placenta, mentre la maggior parte di essi non suole coinvolgere il feto. In ogni modo, però, costituendo la condizione del cancro in gravidanza un’evenienza particolarmente complessa, occorre che essa sia seguita da un team sanitario esperto che definisca l’esatta diagnosi e prognosi, adattando la corretta terapia a ogni specifico caso.
A tale proposito, c’è da considerare come la gravidanza comporti spesso un ritardo nella diagnosi di cancro. Difatti, alcuni sintomi, quali il gonfiore addominale e quello del seno, la frequente cefalea ed anche il sanguinamento rettale, sono spesso trascurati come sospetto della presenza di un cancro perché comuni durante la gravidanza.
Il cancro del collo dell'utero, della mammella, della tiroide, il linfoma di Hodgkin e non-Hodgkin, le leucemie, il melanoma e il tumore trofoblastico gestazionale sono le forme più frequenti durante la gravidanza.
Molto più comune è il cancro al seno che colpisce circa una su 3.000 gravidanze. Da notare, a suo riguardo, che il relativo aumento di turgore del seno della gravida può, peraltro, rendere difficile l'individuazione delle forme di piccole dimensioni, determinando, così, un ritardo di diagnosi di circa quattro mesi, rispetto alle donne non gravide.
Le radiazioni diagnostiche a raggi X, usate per accertare la presenza di neoplasia in gravidanza, destano, invero, preoccupazioni per il possibile danno che può derivare al feto. Possono, difatti, determinare anomalie del frutto di concepimento, diminuzione del quoziente intellettivo e tumori infantili. Tuttavia, la ricerca ha dimostrato che il loro livello è in genere troppo basso per un danno sicuro. In particolare, la tomografia computerizzata (TC) è simile ai raggi X perché utilizza radiazioni ionizzanti, ma offre dati più precisi per delineare gli organi e le strutture interne e può condurre a una diagnosi di sede e di diffusione del cancro in maniera più precisa. In tal caso, la TC della testa o quella del torace sono generalmente considerate sicure durante la gravidanza poiché non vi è alcuna esposizione di radiazione diretta al feto. Per quanto riguarda, invece, la TC dell'addome o del bacino bisognerebbe utilizzarle solo in assoluta necessità. Nell’uso di queste tecniche diagnostiche, comunque, bisognerebbe ricorrere a una protezione di piombo che ricopra l'addome.
La risonanza magnetica (MRI), l'ecografia e la biopsia, che non utilizzano radiazioni ionizzanti, sono, invece, considerate tecniche diagnostiche sicure durante la gravidanza.
Il trattamento della gestante con cancro, deve selezionare le migliori opzioni, sia per la madre sia per prodotto del concepimento, e può prevedere la chirurgia, la chemioterapia e raramente la radioterapia. Tutto ciò va considerato, tenendo conto dello stadio della gravidanza, delle caratteristiche del tumore ed anche delle decisioni della donna e della sua famiglia. I primi tre mesi di gravidanza sono quelli in cui il trattamento antineoplastico può essere più nocivo per il feto. Spesso, quindi, esso viene ritardato fino il secondo o terzo trimestre di gravidanza. Nelle diagnosi più tardive si può, invece, prendere in considerazione l'induzione del travaglio anticipato o, come nello stadio precoce del cancro della cervice uterina, si conviene di aspettare fino a dopo il parto.
Il cancro al seno di solito è trattato chirurgicamente con la chemioterapia adiuvante. La chemioterapia, però, può essere considerata nel secondo e terzo trimestre e i trattamenti radioterapici e ormonali devono essere rimandati nel post-parto.
La gestione dei tumori ovarici è solitamente chirurgica con seguito di chemioterapia. Quella dei tumori ematologici è comunemente chemioterapica.
In generale, nel primo trimestre, per permettere un'adeguata assistenza oncologica, bisogna considerare l'interruzione della gravidanza. Dopo la 24^ settimana, quando la gravidanza raggiunge l'età gestazionale della redditività del feto, bisogna decidere per quanto tempo il trattamento può essere ritardato e in quanto tempo il parto può essere indotto. Prima dell’ottava settimana il trattamento oncologico comporta, di certo, il rischio di malformazioni.
L'allattamento al seno è di norma sconsigliato alle puerpere che sono in trattamento per il cancro, anche se le cellule tumorali non possono passare al bambino attraverso il latte materno. I farmaci chemioterapici, invece, possono giungere al bambino attraverso il latte materno, rappresentando un serio pericolo per la sua salute. Così pure avviene per i componenti radioattivi, come lo iodio radioattivo usato nel trattamento del cancro della tiroide che può essere trasferito al bambino attraverso il latte materno.
C’è da notare che allo stesso modo la prognosi per una gravida non è diversa da quella di una donna non incinta della stessa età con ugual tipo del tumore allo stesso stadio. Per alcuni tipi di cancro, però, la prognosi è peggiore per effetto degli ormoni prodotti in gran quantità durante la gravidanza, avendo gli stessi un particolare potenziale sulla crescita e sulla diffusione della malattia.
Come riferimento a quanto riportato, Salani R dell’Ohio State University Medical Center, Columbus e collaboratori hanno voluto fornire una rilevante panoramica della letteratura attuale nei riguardi della complessa associazione patologica del cancro in gravidanza, descrivendo le opzioni di gestione in rapporto alla salute materna e a quella del feto (Am J Obstet Gynecol. 2014; 211 (1):7-14).
La "Precision Medicine in Cancer Care" al 39° congresso ESMO
Oggetto del 39° Congresso ESMO (European Society for Medical Oncology) a Madrid, sono le difficoltà pratiche incontrate dai ricercatori e medici per l'integrazione della medicina di precisione nella gestione oncologica, compresa la diversa gamma degli effetti collaterali associati alle nuove terapie, come l’immunoterapia e la farmacogenetica.
L’immunoterapia è una delle strategie antitumorali che utilizza un approccio relativamente nuovo per il trattamento del cancro e che promette di trasformare la vita dei pazienti. Ci sono diversi tipi d’immunoterapia ciascuno dei quali lavora in un modo diverso per indurre il sistema immunitario del paziente a distruggere il tumore.
Rolf A. Stahel dell’University Hospital Zurich, Switzerland e attuale presidente dell’ESMO ha dichiarato che l'immunoterapia rivoluzionerà il trattamento del cancro, destinato a cambiare in modo decisivo e sostanziale con le nuove possibilità. Tutto ciò si realizzerà non per una sola malattia, ma per molti tipi di cancro. È certo oramai che l'immunoterapia sta rapidamente emergendo con grande forza di affermazione in oncologia. Peraltro, anche le terapie che interessano le cellule T rappresentano un altro settore emergente. Risposte incoraggianti sono state osservate con la terapia delle cellule T adottive nei tumori ematologici, nel linfoma e nella leucemia, ma anche nei tumori solidi come il melanoma e il sarcoma. Ricerche sono anche in corso in diverse altre aree di malattia, come il cancro alla prostata e al seno. Inoltre, anche lo sviluppo dei vaccini e degli antigeni tumorali è un campo in ascesa di ricerca con aspettative promettenti. Gli studiosi sono fiduciosi che l’immunoterapia possa sfruttare la possibilità di attivare il sistema immunitario in modo robusto contro le cellule tumorali.
In ogni modo, la genomica sta offrendo informazioni sulla genetica dell’iniziazione e dello sviluppo del cancro, fondamentali per la realizzazione della terapia personalizzata. Quest’aspetto di ricerca permette di promuovere lo sviluppo di molte altre terapie antitumorali. Pu tuttavia, il progresso nella lotta contro il cancro deve sempre mirare alla più attenta prevenzione e alla precocità d’individuazione, di diagnosi di cura della malattia.

