Note introduttive degli effetti endocrino - metabolici della metformina
La metformina è un farmaco ipoglicemizzante orale biguanide utilizzato per decenni per il trattamento del diabete di tipo 2. Recenti studi hanno indicato che migliora anche le anomalie delle donne con sindrome dell'ovaio policistico, intervenendo con la diminuzione dei livelli degli androgeni, con la regolarizzazione del ciclo mestruale e della funzione ovulatoria. Inoltre, corregge la dislipidemia, comunemente associata con la sindrome.
Il farmaco, in effetti, aumenta il numero dei recettori dell’insulina nel tessuto muscolare e adiposo e l'attrazione verso di essi. Non incrementa la secrezione dell’insulina, ma solo la sensibilità a essa. Pertanto, non tende a causare ipoglicemia.
La sua attività riduce, in definitiva, i livelli dell’ormone, aumenta la sensibilità dei tessuti periferici ai suoi effetti, rinvigorisce la sua risposta e ripristina i suoi livelli ematici fisiologici con quelli del glucosio e può anche produrre la perdita del peso corporeo e certamente la diminuzione del contenuto del grasso totale.
La metformina aumenta anche la sensibilità ipotalamo-ipofisaria agli effetti dell’insulina. In effetti, questa condizione suole ridursi con l'età provocando gli elevati livelli dell’ormone nel sangue. Tutto ciò, com’è noto, si associa, quindi, a un certo numero di effetti nocivi accelerati dall’età.
In sintesi, questi stessi corrispondono a un incremento delle infezioni, all’ipercolesterolemia, all’ipertensione, all’aterosclerosi precoce, all'obesità e alle complicanze microvascolari, come la retinopatia, la nefropatia, le neuropatie.
Di recente Szu-Chun Hung del Taipei veterans general hospital di Taiwan e collaboratori, sulla base delle evidenze sull'uso prudente della metformina nei soggetti con malattia renale cronica lieve-moderata, considerando, tuttavia, carenti gli studi nei meriti, hanno voluto valutarne per loro conto la sicurezza nei pazienti con diabete di tipo II e con malattia renale cronica avanzata in fase 5 (Lancet Diab Endoc 2015. doi: 10.1016/S2213-8587 (15)00123-0).
Gli Autori hanno, così, condotto uno studio osservazionale di coorte di pazienti con diabete di tipo 2 che erano stati arruolati prospetticamente nei database di ricerca nazionale di Taiwan da parte dell’assicurazione sanitaria tra il gennaio 2000 e il 30 giugno 2009 con follow-up fino al 31 dicembre 2009. Erano inclusi individui con una concentrazione di creatinina sierica superiore a 530 micromol / L, dato approssimativamente equivalente alla fase cinque della malattia renale cronica. Da un campione consecutivo di 12.350 pazienti con diabete di tipo 2 e malattia renale cronica, 1.005 avevano utilizzato la metformina e 11.345 erano non-utenti. Si abbinavano gli utenti e i non utenti del farmaco con un punteggio di propensione in un rapporto di 1: 3. L’outcome primario consisteva nella mortalità.
Il totale di 813 utenti era abbinato per punteggio di propensione con 2.439 non utenti. I due gruppi di pazienti non differivano significativamente da trenta variabili di base cliniche e socio-economiche. Il follow-up nella coorte era di 2,1 anni (range 0,3-9,8). La mortalità era riportata in 434 (il 53%) degli 813 utenti e in 1.012 (il 41%) dei 2.439 non utenti. Dopo aggiustamento multivariato, l'uso della metformina si dimostrava un fattore di rischio indipendente di mortalità (hazard ratio aggiustato 1 • 35, IC 95%= 1,20-1,51; p <0, 0001). Il rischio di mortalità maggiore era dose-dipendente ed era coerente in tutte le analisi dei sottogruppi. Tuttavia, l'uso della metformina, rispetto al non uso, era associato a un rischio più elevato, ma non significativo, di acidosi metabolica (1,6 vs 1,3 eventi per 100 pazienti-anno; hazard ratio aggiustato 1,30, IC 95%= 0,88- 1,93; p = 0, 19).
In conclusione, l'uso della metformina nelle persone con diabete di tipo 2 con una concentrazione di creatinina sierica superiore ai 530 micromol / L si associava a un aumento significativo del rischio di mortalità per tutte le cause, rispetto ai non utilizzatori. Pertanto, secondo gli Autori, l’uso del farmaco non doveva essere incoraggiato in questo gruppo di pazienti.
Metformina (glucophage) e diabete mellito gestazionale
Il GDM (Gestational Diabetes Mellitus) è carattherizzato da un qualsiasi grado d’intolleranza al glucosio con insorgenza in gravidanza, o inizialmente individuato nel suo decorso. Recentemente la sua incidenza complessiva è stata riportata in aumento, verosimilmente in rapporto alla maggiore età attuale delle donne incinte e alla maggiore prevalenza dell’obesità. Pur tuttavia, il dato varia ampiamente in rapporto ai criteri diagnostici e alle caratteristiche della popolazione studiata, come ad esempio l’etnia. I tassi di prevalenza sono riportati, in effetti, più elevati nelle isole del pacifico, negli individui di colore non ispanici e nelle popolazioni ispaniche, rispetto ai bianchi non ispanici. In particolare, negli Stati Uniti la prevalenza del GDM va dall’1,1 al 25,5% di tutte le gravidanze e si stima che nei sudamericani e negli indiani sia corrispondente rispettivamente al 2,2% e al 15% delle gravidanze. Il GDM si associa a un aumentato rischio di complicanze materne e perinatali, tra cui la preeclampsia, il parto cesareo, la macrosomia, le lesioni e i traumi alla nascita, la prematurità, l’ipoglicemia e il distress respiratorio neonatale. D’altra parte, diversi studi hanno ormai dimostrato che il rischio degli esiti negativi in gravidanza aumenta continuamente in proporzione agli elevati livelli del glucosio e che esso può essere ridotto con un efficace trattamento. Difatti, gli interventi rivolti a modificare lo stile di vita hanno dimostrato di migliorare i risultati perinatali. In caso di persistenza dell’iperglicemia, però, i trattamenti aggiuntivi, tradizionalmente l'insulina, devono essere spesso attivati. Pur tuttavia, la terapia insulinica, se efficace per un verso, dimostra, però, diversi svantaggi per la gravida, tra cui le iniezioni multiple giornaliere, il rischio dell’ipoglicemia, l’aumento del peso corporeo e l’incremento dei costi sanitari. Inoltre, richiede regolazioni in base al peso della madre, ai livelli della glicemia e alla dieta e all'attività fisica, che obbligano, quindi, a valutazioni frequenti. Sotto tali aspetti, un agente orale sicuro ed efficace avrebbe rispetto all'insulina un indiscusso vantaggio. La metformina, come farmaco di prima linea per diabete di tipo 2 nelle pazienti non gravide, nel GDM si offre sicuramente come ottimale candidato farmacologico. Difatti, riduce la gluconeogenesi epatica e migliora l'assorbimento del glucosio periferico senza associarsi a un aumento del peso o all’ipoglicemia. La metformina attraversa la placenta con una velocità di trasferimento materno-fetale stimato dal 10 al 16%, in modo che si può influenzare direttamente la fisiologia del feto. Gli effetti a lungo termine del farmaco sui disturbi metabolici futuri nella prole sono al momento sconosciuti e costituiscono una barriera importante per il suo uso. Tuttavia, si è ipotizzato che la metformina induce un ambiente intrauterino più favorevole e può ridurre nella prole le complicanze metaboliche a lungo termine, come l'obesità o lo stesso diabete mellito.
Lautatzis ME dell’Aristotle University of Thessaloniki, Greece e collaboratori, attraverso una revisione narrativa per fornire chiarimenti sull'uso della metformina in gravidanza, hanno valutato criticamente le evidenze emerse in letteratura sulla sua efficacia e sicurezza di uso (Metabolism. 2013 Nov;62 (11):1522-34).
La metformina sembrava essere efficace e sicura per il trattamento del diabete mellito gestazionale (GDM), in particolare nelle donne in sovrappeso o obese. Tuttavia, le pazienti con fattori di rischio multipli per la resistenza all'insulina non potevano soddisfare i loro obiettivi di trattamento con la sola metformina e potevano richiedere un supplemento insulinico. L'evidenza suggeriva che nel GDM, rispetto all’insulina, c’erano con l'uso del farmaco, nei riguardi del peso della madre e degli esiti neonatali, maggiori vantaggi potenziali. Inoltre, le pazienti accettavano maggiormente la metformina piuttosto che l'insulina. L'uso del farmaco durante la gravidanza nelle donne con sindrome dell'ovaio policistico riduceva i tassi d’interruzione della gravidanza precoce e del parto pretermine e proteggeva contro la restrizione della crescita fetale. Inoltre, non si dimostravano con l'uso della metformina gli effetti teratogeni, i decessi intrauterini, o i ritardi dello sviluppo.
In conclusione, le pubblicazioni, recensite nell’articolo sui risultati immediati durante la gravidanza, supportavano l'efficacia e la sicurezza della metformina. Peraltro, poiché non vi erano linee guida per l'uso continuo del farmaco in gravidanza, la durata del trattamento si basava caso per caso sul giudizio clinico e sull'esperienza professionale.
Per loro conto, Zhuo Z della Southern Medical University, China e collaboratori hanno effettuato una meta-analisi sull'effetto della metformina nella GDM del PCOS, valutando se potesse ridurre con un modello di effetti fissi l’occorrenza dello stesso disturbo metabolico (J Diabetes Res. 2014;2014:381231).
Era calcolato l'odds ratio (OR) con il 95% d’intervallo di confidenza (IC 95%) per stimare la forza dell'associazione. Erano, così, inclusi tredici studi di cui cinque RCT e otto no.
In definitiva, l'analisi dimostrava in totale che negli RCT non vi era alcuna efficacia significativa della metformina sulla GDM nella PCOS, rispetto al placebo (OR = 1,07, 95% IC 0,60-1,92), e solo nei non RCT una significativa disponibilità sulla GDM (OR = 0.19, IC 95%= 0,13-0,27).
In conclusione, in base ai risultati della meta-analisi, la metformina non aveva un impatto significativo sulla GDM nella PCOS.
Bijok J dell’Ortowskiego w Warszawie, Polska e collaboratori, proprio perché la metformina attraversa la placenta, hanno prodotto una recensione sulla possibilità dei suoi effetti negativi sul feto, discutendo ampiamente sulla sua sicurezza e sulle sue indicazioni di somministrazione in gravidanza (Ginekol Pol. 2014 Jul;85 (7):527-31).
Per loro conto, Pedro Marques dell’Hospital de Santa Maria, CHLN, Lisboa, Portugal e collaboratori hanno voluto valutare nel GDM (gestational diabetes mellitus) la sicurezza materna e neonatale della metformina (Endocr Pract. 2014;20 (10):1022-1031).
Gli Autori ritenevano, infatti, che, nonostante le crescenti relazioni sulla sua sicurezza ed efficacia, l'uso del farmaco nelle donne gravide fosse ancora controverso.
Si analizzavano, quindi, retrospettivamente le cartelle cliniche di 186 gravidanze complicate con GDM, sorvegliate all'ospedale di appartenenza tra il 2011 e il 2012. Di poi, si confrontavano gli esiti materni e neonatali durante la gravidanza di trentadue donne in trattamento con la metformina con 121 femmine controllate con la dieta e con trentatré trattate con l’insulina.
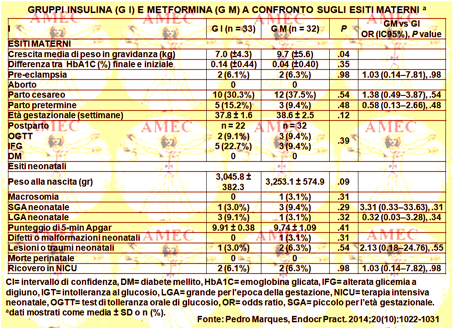
Delle 186 donne con GDM 32, il 17,2%, avevano ricevuto la metformina durante la gravidanza. Non si riscontava nessuna differenza statistica tra il gruppo sotto dieta e quello con metformina, per quanto riguardava i tassi di aborto, di prematurità, di preeclampsia, di macrosomia, di SGA (small-for-gestational-age) o di LGA (largefor-gestational-age) neonatale, di parti cesarei, di ammissioni UTIN (neonatal intensive care unit) e di malformazioni o lesioni neonatali alla nascita. Allo stesso modo, non vi erano differenze tra i gruppi della metformina e dell’insulina, per quanto riguardava i risultati riferiti. Non si registravano aborti o morti perinatali nel gruppo metformina. In particolare, dieci su trentadue pazienti con metformina imponevano la necessità dell’insulina supplementare.
In conclusione, questo studio retrospettivo suggeriva che la metformina si proponeva come una sicura alternativa o trattamento aggiuntivo all'insulina nelle donne con GDM, non avendo dimostrato, rispetto ai gruppi dell’insulina o della dieta, alcuna associazione a un più alto rischio di complicanze materne o neonatali.
V. R. Aroda del MedStar Health Research Institute, Hyattsville, Maryland e collaboratori, considerando che nel DPP (Diabetes Prevention Program) il GDM (Gestational diabetes) conferiva un alto rischio di diabete di tipo 2, ostacolato nella sua comparsa dall’ILS (intensive lifestyle) e dalla metformina, hanno voluto valutare in dieci anni l'impatto di questi due interventi nelle donne con e senza una storia di GDM (J Clin Endocrinol Metab. 2015 Apr;100 (4):1646-53).
Il DPP, com’è noto, è stato uno studio randomizzato di persone in sovrappeso o obese ad alto rischio di diabete di tipo 2, assegnate a cambiare lo stile di vita intensamente, con l’obiettivo della perdita di peso del 7%. Si aggiungevano 150 minuti o più a settimana di esercizio fisico di moderata intensità, 850 mg di metformina due volte il giorno, o il placebo.
Gli Autori, quindi, in ventisette centri clinici hanno approntato uno studio randomizzato e controllato con un follow-up osservazionale.
Si arruolavano, così, trecentocinquanta donne con una storia di GDM e 1.416 con precedenti nati vivi, ma senza storia di GDM. All'inizio dello studio, le partecipanti avevano un elevato indice di massa corporea, un’alta glicemia a digiuno e una ridotta tolleranza al glucosio.
Gli interventi includevano il placebo, l’ILS o la metformina, mentre la misura degli esiti era rappresentata dal diabete mellito.
In dieci anni le donne con la storia di GDM assegnate al placebo avevano un rischio maggiore del 48% di sviluppare il diabete rispetto ai controlli. Nelle donne con una storia di GDM, l’ILS e la metformina, rispetto al placebo, riducevano la progressione verso il diabete, rispettivamente del 35% e del 40%. Tra le donne senza una storia di GDM, l’ILS riduceva la progressione verso il diabete del 30%, mentre la metformina non aveva questo effetto.
In conclusione, le donne con una storia di GDM erano ad aumentato rischio di sviluppare il diabete. Nel DPP / Diabetes Prevention Programma Outcomes Study le donne con una storia di GDM trovavano grande efficacia sia nello stile di vita e sia nella metformina. Si otteneva, difatti, durante un periodo di follow-up di dieci anni la riduzione della progressione verso il diabete. Tra le donne senza una storia di GDM, lo stile di vita, ma non la metformina, riduceva la progressione verso il diabete.
Per loro conto, Yun-fa Jiang dell’Hebei Medical University, China e collaboratori, per valutare l'efficacia e la sicurezza degli OAD (oral antidiabetic drugs) nel diabete gestazionale, hanno condotto una meta-analisi sui dati della letteratura sino all’ottobre 2014 (J Clin Endocrinol Metab. 2015 Mar 24: jc20144403).
Gli Autori includevano, così, diciotto RCT e confermavano che non c’era nessuna differenza significativa nella glicemia o nella HbA1c nelle pazienti trattate con l'insulina, con la metformina e con la gliburide. Rispetto all'insulina, la metformina si associava, però, a un più basso aumento del peso materno (WMD: -1.49 kg, IC 95%: -2,26 a -0,31), a un’età gestazionale inferiore (WMD: -0.16 settimane, IC 95%: -0,30 a -0,03) e a una maggiore incidenza di prematurità (OR: 1,63, IC 95%: 1,07-2,48). La gliburide, invece, si associava a un peso alla nascita neonatale più alto (WMD: 130,68 g, IC 95%: 55,98 per 205,38), a un’aumentata incidenza d’ipoglicemia neonatale (OR: 2,64, IC 95%: 1,59-4,38) e di macrosomia (OR: 3,09, IC 95%: 1,59-6,04). La metanalisi rivelava anche che la gliburide, rispetto alla metformina, si associava a una maggiore incidenza dell’ipoglicemia neonatale e della macrosomia, del peso materno e del neonato alla nascita.
In conclusione, tenuto conto del buon controllo glicemico, sia la metformina e sia la gliburide si dimostravano adatte per la gestione del diabete gestazionale. Tuttavia, la gliburide dimostrava un aumento del rischio dell’ipoglicemia neonatale, dell’elevato incremento del peso materno e della macrosomia alla nascita.
Alla luce di quanto evidenziato dalle ricerche scientifiche, Carolyn A Chiswick dell’University of Edinburgh, UK e collaboratori hanno presentato un protocollo di studio per testare come la metformina potesse migliorare la sensibilità all’insulina nelle gravide obese, riducendo, così, l'incidenza dell’alto peso alla nascita e di altre complicazioni durante la gravidanza (BMJ Open 2015;5: e006854).
L’indicazione traeva spunto dalle suggestive e crescenti evidenze sulle origini dell'obesità prima della nascita. In effetti, gli Autori facevano rilevare la chiara correlazione tra l’obesità materna, l’alto peso alla nascita e il rischio dell’obesità della prole nell’età adulta. Era annotata anche la correlazione tra le gravide obese e il maggior rischio degli esiti avversi, tra cui il diabete gestazionale e la natimortalità. Tra i meccanismi possibili di tali condizioni, l’iperglicemia e l'insulino-resistenza avrebbero dovuto dimostrare una forte connessione.

L’EMPOWaR (Efficacy of Metformin in Pregnant Obese Women, a Randomised Controlled Trial) dovrebbe stabilire l'efficacia della metformina nelle donne obese in gravidanza. Lo studio randomizzato e controllato in doppio cieco con placebo dovrebbe, in effetti, determinare se il farmaco abbia la proprietà di ridurre l'incidenza dell’alto peso dei bambini alla nascita. Come obiettivo secondario si prefigge di testare gli effetti secondari del farmaco.
Gli Autori hanno affermato che questo sarebbe il primo studio multicentrico, in doppio cieco, randomizzato e controllato per esaminare l'effetto della metformina in donne in gravidanza, obese ma senza diabete.
Nello stesso ordine d’intenti, Ainuddin JA della Dow University of Health Sciences, Karachi e collaboratori, per valutare l'effetto della metformina nel controllare il GDM (Gestational Diabetes Mellitus) nelle donne con PCOS (Polycystic Ovarian Syndrome), hanno svolto uno studio di coorte comparativo dal 2008 al 2010 (J Coll Physicians Surg Pak. 2015 Apr;25 (4):237-41).
Gli Autori raggruppavano in due bracci le pazienti con diagnosi di PCOS con iperinsulinemia in previsione di gravidanza:
- 50 pazienti con metformina durante la gravidanza,
- 32 pazienti senza metformina.
Lo sviluppo del GDM era accertato in entrambi i gruppi e le pazienti erano seguite per tutta la gravidanza e in puerperio con OGTT secondo i criteri della WHO. La misura dell’esito primario consisteva nello sviluppo del diabete mellito gestazionale.
Un totale di ottantadue donne con PCOS era, quindi, incluso in questo studio, nel quale, come specificato, cinquanta ricevevano il trattamento con metformina, mentre trentadue ne erano esentate. Le donne in gravidanza in entrambi i gruppi con sindrome dell'ovaio policistico erano comparabili per età, peso, parità e BMI. All’inizio dello studio i livelli medi dell’insulina a digiuno erano 17,22 ± 2,3 mIU / L nel gruppo metformina e 16.93 ± 2.28 mIU / L in quello senza il farmaco (p = 0,589). I livelli medi dello zucchero nel sangue a digiuno erano 94.54 mg / dl nel gruppo con metformina e 99.59 mg / dl in quello del controllo con p <0,001. Un totale di 5 (10%) pazienti del gruppo metformina sviluppava GDM, mentre 11 (34.37% OR 4,71, p = 0.01) nella controparte. Le pazienti non trattate con metformina mostravano, quindi, 4,7 volte maggiori probabilità di sviluppare il GDM (OR: 4,71), rispetto a coloro che la ricevevano.
In conclusione, La frequenza del diabete gestazionale era significativamente più alta nelle pazienti con PCOS che non ricevevano metformina, rispetto a coloro che lo avevano fatto.
Metformina e malattia dell’ovaio policistico
La metformina ha dimostrato di essere anche utile nel ridurre l’iperinsulinemia e l’iperandrogenismo nelle pazienti con PCOS (polycystic ovarian syndrome). Essa da una parte migliora la risposta all'insulina durante la tolleranza orale al glucosio e dall’altra, come altri sensibilizzatori dell'insulina, agisce direttamente sulle cellule tecali con diminuzione della produzione degli steroidi. I vantaggi della metformina sono stati ampiamente studiati nelle donne infertili con diagnosi di PCOS, in cui la causa primaria della sterilità è di solito la mancanza della regolare ovulazione. In tali casi il citrato di clomifene, somministrato per indurre la crescita del follicolo, è il farmaco tipico di prima linea. Pur tuttavia, la metformina è spesso prescritta per aiutare l'ovulazione, anche se studi randomizzati non hanno mostrato risultati superiori, rispetto al clomifene.
La sindrome dell'ovaio policistico (PCOS), diagnosticabile sino al 14 per cento della popolazione femminile in età fertile, è l'anomalia endocrina più comune delle donne in età riproduttiva. Essa è classicamente caratterizzata da: iperandrogenismo, anovulazione cronica, morfologia ovarica policistica valutabile all’esame ecografico. Anche se i meccanismi fisiopatologici alla base della PCOS rimangono poco chiari, l'insulino-resistenza (IR), intrinseca alla sindrome, sembra svolgere un ruolo centrale nel suo sviluppo.
Il fegato e i muscoli scheletrici sono, in effetti, resistenti alle azioni dell’insulina, così che, al fine di mantenere l’euglicemia, viene prodotta un’eccessiva quantità dell’ormone. L'insulina e l’IGF (insulin-like growth factor), però, agiscono anche come fattori di crescita nelle ovaie, stimolando la sintesi degli androgeni, responsabili dell’irsutismo, dell’acne ed anche del blocco di sviluppo del follicolo. Peraltro, oltre il 50% delle donne con PCOS sono in sovrappeso o obese, il che aumenta ulteriormente la loro resistenza all'insulina.
Quest’ultima condizione, se non trattata, può concludersi, quindi, con l’intolleranza al glucosio e anche con il diabete di tipo 2 e con le malattie cardiovascolari.
Erin K. Barthelmess e Rajesh K. Naz della West Virginia University School of Medicine, Health Sciences Center, Morgantown nella loro revisione hanno proprio discusso lo stato attuale e la possibile prospettiva futura della PCOS (Frontiers In Bioscience, Elite, E6, 104 - 119, January 1, 2014).
Gli Autori hanno, difatti, ribadito che la sindrome dell'ovaio policistico è una patologia riproduttiva diffusa, comprendente molte condizioni di salute associate a essa. Essa è stata descritta con un impatto sui vari processi metabolici. È rappresentata dall’iperandrogenismo, dalle ovaie policistiche e dall’anovulazione con aumento del rischio di resistenza all'insulina (IR), del diabete di tipo 2, dell'obesità e delle malattie cardiovascolari. Gli Autori, confermando un'eziologia poco chiara, hanno ribadito l’esistenza di un fenotipo soggettivo che determina tra i medici una diagnosi unitaria difficile. Nel suo caso è stata definita come possibile sindrome genetica familiare causata da una combinazione di fattori ambientali e genetici. Può essere collegata a disturbi metabolici in familiari di primo grado. La PCOS, comunque, anche per gli Autori è stata considerata la causa fino al 30% dell’infertilità nelle coppie in cerca di trattamento con mancanza attuale di cure risolutive.
Lourdes Ibáñez dell’University of Barcelona, Spain e collaboratori hanno voluto confrontare la capacità della metformina nel prevenire la PCOS delle adolescenti con una storia combinata di basso LBW (low (-normal) birth weight) e PP (precocious pubarche) ad alto rischio di sviluppare la sindrome (J Clin Endocrinol Metab 96: E1262–E1267, 2011).
Le premesse degli Autori erano basate sulle evidenze che tendevano a indicare come un eccesso di lipidi nel tessuto adiposo delle adolescenti e delle giovani donne potesse rappresentare un’importante origine dell’eccesso degli androgeni. Tale condizione, in effetti, poteva derivare da una combinazione di una normale capacità di riserva dei lipidi con uno squilibrio cronico di energia positiva, come nella semplice obesità, o di una bassa capacità di stoccaggio dei lipidi con un normale apporto energetico, come nelle lipodistrofie genetiche, oppure di una bassa-normale capacità di stoccaggio con un apporto energetico alto-normale, come nelle ragazze che conciliano un basso-normale peso alla nascita con un elevato-normale indice di massa corporea (BMI)]. Gli Autori riproponevano che l’ultimo sottogruppo era in particolare e rapida espansione potendo divenire ormai il più grande su scala globale, non tanto perché stesse riducendosi il peso alla nascita, ma perché era in aumento la BMI anche in popolazioni con una bassa capacità di accumulo dei lipidi. Il pubarca precoce e la comparsa dei peli al pube prima degli otto anni erano, peraltro, un punto di riferimento classico della sequenza da un LBW (low birth weight) a un menarca precoce e quindi più avanti verso un fenotipo PCOS e una altezza da adulte sotto il livello medio parentale.
Gli Autori avviavano, così, uno studio randomizzato in aperto di oltre sette anni su una coorte di ragazze con LBW-PP per esplorare il potenziale della metformina nel prevenire o ritardare lo sviluppo della PCOS. Nei primi anni di questa ricerca osservavano che la terapia precoce con metformina si accompagnava con una riduzione del grasso viscerale ed epatico, con un menarca meno avanzato e con una statura più alta.
In particolare, trentotto ragazze LBW-PP erano seguite dall'età media di otto anni fino ai 15 con confronto tra l’intervento di metformina precoce di 1-4 anni agli 8-12 anni, vs. quello tardivo di 6 anni nell’età di 13-14.
Le principali misure dopo sette anni di esito includevano in tutte le ragazze, non trattate così per almeno un anno,: l’altezza, il peso, il punteggio dell’irsutismo, il ciclo mestruale, i dati endocrino-metabolici di screening a digiuno e nella fase follicolare, la Proteina C-reattiva, la composizione corporea, la distribuzione del grasso addominale con la risonanza magnetica, la morfologia ovarica con gli ultrasuoni, la PCOS come definita dal National Institutes of Health and Androgen Excess Society.
Nessuna delle ragazze usciva dallo studio e a quindici anni quelle trattate con metformina precoce erano più alte di 4 cm, mostravano uno stato pro-infiammatorio più basso e avevano un minore grasso centrale dovuto alla riduzione di quello viscerale ed epatico. L’irsutismo, l’eccesso di androgeni, l’oligomenorrea e la PCOS erano più prevalenti tra le due e le otto volte nelle ragazze con trattamento tardivo rispetto a quelle precoce. L’adiposità addominale era la prima variabile a divergere tra le ragazze con PCOS a 8-10 anni di età, rispetto a quelle senza a quindici anni.
In conclusione, nelle ragazze LBW-PP la terapia precoce con metformina dimostrava di prevenire o ritardare lo sviluppo dell’irsutismo, dell’eccesso di androgeni, dell’oligomenorrea e della PCOS più efficacemente di quella tardiva. Peraltro, la finestra temporale della tarda infanzia e della pubertà precoce poteva essere più critica per la sviluppo e, quindi, per la prevenzione della PCOS nelle adolescenti rispetto ai primi anni successivi al menarca.
Dal loro canto, Hamidreza Mani del Leicester General Hospital, UK e collaboratori, per verificare l'incidenza e la prevalenza degli eventi cardiovascolari in una coorte di donne con PCOS, hanno svolto uno studio di coorte retrospettivo con follow-up totale maggiore di 12.000 persone-anno (Clin Endocrinol, Volume 78, Issue 6 June 2013, Pages 926–934).
Gli Autori ritenevano che il potenziale aumento del rischio delle malattie cardiovascolari nelle donne con sindrome dell'ovaio policistico (PCOS), dovuto alla resistenza all'insulina, all’obesità e al diabete di tipo 2 (DM2), non fosse stato in questa popolazione ancora sufficientemente dimostrato.
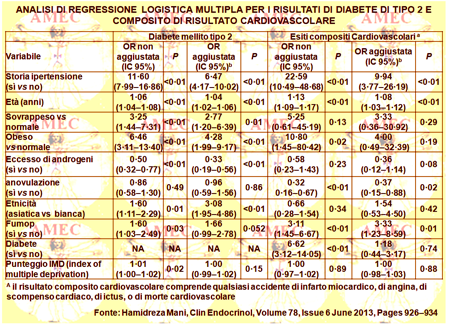
Si arruolavano, così, 2.301 donne con PCOS di età media di 29,6 anni, che frequentavano una clinica di specialità nel Leicestershire nel Regno Unito.
Come principali risultati, occorrevano il diabete di tipo 2, l’infarto del miocardio (IMA), l’angina, l’insufficienza cardiaca (HF), l’ictus e la morte cardiovascolare correlata.
L’incidenza di questi incidenti patologici era rispettivamente 3.6, 0.8, 1.0, 0.3, 0.0 e 0.4 per 1000 anni-persona. Alla fine del follow-up la prevalenza dell’IMA nelle fasce di età dai quarantacinque ai cinquantaquattro, dai cinquantacinque ai sessantaquattro e oltre i sessantacinque anni era corrispondente allo 1.9%, al 6.0% e al 27.3%. Per l’angina corrispondeva rispettivamente al 2.6%, al 6.0% e al 27.3%. Gli odds ratio, specifici per i gruppi di età per la prevalenza dell’infarto miocardico e dell’angina, rispetto alla popolazione femminile locale, erano compresi tra 2.6 (IC 95%: 1.0-6.3) e 12.9 (IC: 3.4-48.6). Il più alto rapporto si otteneva nel gruppo oltre i sessantacinque anni per l’IMA. Nelle pazienti con PCOS l'età, la storia d’ipertensione e il fumo avevano correlazioni significative con gli esiti cardiovascolari.
In conclusione, nelle donne con sindrome dell'ovaio policistico si dimostravano un'alta incidenza e prevalenza specifica per l’età, per il diabete di tipo 2, per l’IMA e per l’angina. In particolare, più di un quarto delle ultra sessantacinquenni aveva presentato un infarto miocardico o un’angina. Secondo gli Autori, questi risultati dovevano certamente essere considerati nelle donne con PCOS per le strategie di trattamento e di pianificazione a lungo termine.
Per loro conto, Roger Hart e Dorota A. Doherty dell’University of Western Australia, Perth hanno eseguito uno studio retrospettivo di coorte, basato sulla popolazione, su un totale di 2.566 donne con PCOS ospedalizzate dal 1997 al 2011 e su 25.660 donne di pari età senza la sindrome, selezionate in modo casuale, (The Journal of Clinical Endocrinology & Metabolism, 2014; jc.2014-3886).
La principale misura di esito consisteva nel confronto dei ricoveri di quindici anni, seguiti fino a una media di 35,8 (range interquartile= 31,0-39,9).
La PCOS era caratterizzata da un maggior numero di ricoveri ospedalieri di tipo non ostetrico e non legati a infortuni (media 5 vs 2; P <.001), di diagnosi di diabete dell'adulto (12,5 vs 3,8%), di obesità (16,0 vs 3,7%), d’ipertensione (3,8 vs 0,7%), di cardiopatia ischemica (0,8 vs 0,2%), di malattia cerebrovascolare (0,6 vs 0,2%), di malattia venosa e arteriosa (0,5 vs 0,2% e 10,4 vs 5,6%, rispettivamente), di asma (10.6 vs 4.5%), di stress / ansia (14,0 vs 5,9%), di depressione (9,8 vs 4,3%), di uso di droga (8,8 vs 4,5%), di autolesionismo (7,2 vs 2,9%), d’incidenti di trasporto terrestre (5.2 vs 3,8%) e di mortalità (0,7 vs 0,4%) (P <.001). Le donne con PCOS avevano un più alto tasso di ricoveri per menorragia (14,1 vs 3,6%), di trattamento della sterilità (40,9 vs 4,6%) e di aborto spontaneo (11,1 vs 6,1%). Richiedevano anche con maggiore probabilità la fecondazione in vitro (17,2 vs 2,0%).
In conclusione, la PCOS implicava profonde conseguenze mediche per la salute delle donne, che richiedevano consequenziali massime quote di risorse sanitarie.
Peraltro, Richard S. Legro del Penn State University College of Medicine e collaboratori hanno formulato, per conto dell’Endocrine Society, le linee guida per la diagnosi e il trattamento della PCOS (J Clin Endocrinol Metab 98: 4565–4592, 2013).
Gli Autori consigliavano di considerare la presenza di due tra i criteri di Rotterdam per la diagnosi di PCOS: l’eccesso di androgeni, la disfunzione ovulatoria, o l’ovaio policistico.
Si ribadiva che la diagnosi era problematica nelle adolescenti e nelle donne in menopausa. Nelle prime, comunque, l’iperandrogenismo era centrale per la presentazione, mentre per le seconde non vi era alcun fenotipo coerente. Pur tuttavia, la valutazione delle donne affette avrebbe sempre dovuto escludere altre alternative di eccesso di androgeni.
I contraccettivi ormonali rimanevano i farmaci di prima linea per le anomalie mestruali e l’irsutismo / acne. Il clomifene costituiva la terapia di prima linea per l'infertilità. La metformina rappresentava, per suo canto, il rimedio benefico per le anomalie metaboliche e glicemiche e per il miglioramento delle irregolarità mestruali, ma aveva un limitato o nessun beneficio per correggere l’irsutismo, l’acne, o l’infertilità. I contraccettivi ormonali e la metformina riproducevano le opzioni di trattamento nelle adolescenti. La perdita di peso per se migliorava lo stato della PCOS in modo incerto, ma l'intervento sullo stile di vita era, di certo, utile per gli altri benefici per la salute nel sovrappeso / obesità. I tiazolidinedioni presentavano un rapporto totale rischio/beneficio sfavorevole e le statine richiedevano ulteriori studi per una valutazione definitiva.
La presenza dell’IR nella PCOS è, comunque, parzialmente sostenuta dall'obesità, poiché si trova anche nelle donne magre con la sindrome. Dato il notevole onere metabolico dell’IR, le malate possono avere un aumentato rischio di diabete mellito tipo 2, di malattie cardiovascolari e anche di NAFLD (nonalcoholic fatty liver disease).
Alcuni studi e anche metanalisi hanno evidenziato, in effetti, che il farmaco migliorava i tassi di ovulazione rispetto al placebo e che la sua combinazione con il clomifene comportava risultati superiori a questo farmaco da solo. Peraltro, il clomifene e la metformina hanno anche dimostrato un impatto positivo sui tassi di gravidanza e nelle obese con sindrome dell'ovaio policistico. Peraltro, il primo appare più suscettibile di determinare nati vivi, rispetto alla sola metformina.
In particolare, poi, le donne affette da PCOS, che si sottopongono al trattamento di fecondazione in vitro, potrebbero anche ottenere vantaggi dalla somministrazione della metformina. Il dato è riferibile alla consequenziale, significativa riduzione del rischio della sindrome da iperstimolazione ovarica. Peraltro, durante la gravidanza, essendo queste malate ad aumentato rischio di complicanze (diabete gestazionale, complicazioni ipertensive, tossiemia gravidica), l'uso della metformina si è dimostrato sicuro, senza aumento del rischio di anomalie congenite e d’influenza sulla crescita fetale o dello sviluppo postnatale. Inoltre, il farmaco non ha mostrato di incidere sui tassi di aborto spontaneo. L'uso della metformina ha mostrato, invece, un’associazione con un freno dell’aumento del peso materno durante la gravidanza, della più bassa incidenza dell’ipoglicemia e dell’inferiore necessità d’insulina per gestire il diabete gestazionale. Le donne con diabete gestazionale, trattate con metformina, presentavano anche un esito neonatale paragonabile a quelle curate con l'insulina.
Dal loro canto, Attia GR dell’University of Texas Southwestern Medical Center at Dallas, USA e collaboratori hanno trattato cellule umane ovariche similtumorali tecali con varie concentrazioni per quarantotto ore di metformina in presenza e assenza di forskolin. Hanno eseguito tutto questo per esaminare l'effetto diretto del farmaco sulla produzione degli androgeni cellulari (Fertil Steril. 2001 Sep;76 (3): 517-24).
Si raccoglievano, così, per RIA (radioimmunoassay) il progesterone, il 17 OHP (17 alpha-hydroxyprogesterone), l’androstenedione e il testosterone, esaminando l'effetto della metformina sull’espressione dei vari enzimi coinvolti nella steroidogenesi delle cellule tecali.
La metformina (50 microM e 200 microM), e non la forskolina, inibiva significativamente la produzione dell’androstenedione dalle cellule stimolate. La produzione del testosterone era significativamente inibita nelle cellule trattate con forskolina alla presenza di 200 microM di metformina, rispetto a quelle trattate con sola forskolin. L’analisi Western blot rivelava che la metformina inibiva significativamente l'espressione della proteina STAR (steroidogenic acute regulatory) e della CYP17 (17 alpha-hydroxylase) nelle cellule stimolate con forskolin, rispetto al trattamento della sola forskolin. Non c'era alcun cambiamento significativo nell’espressione della proteina 3 beta HSD (3beta-hydroxysteroid dehydrogenase) o del CYP11A1 (cholesterol side-chain cleavage). L’analisi di Northern rivelava una diminuzione significativa dell'espressione del CYP17 mRNA nelle cellule stimolate con forskolina e trattate con metformina (200 microM), rispetto a quelle con sola forskolin. Tuttavia, non vi era alcun cambiamento significativo nell’espressione della proteina mRNA regolatrice acuta steroidea.
In conclusione, i risultati suggerivano che la metformina poteva avere un effetto inibitorio diretto sulla produzione degli androgeni delle cellule tecali, spiegando il meccanismo di riduzione dei livelli degli androgeni con il farmaco.
Zheng J dell’University College of Medicine, Hangzhou, China e collaboratori, rilevando la controversia sul ruolo della metformina nel trattamento di donne in gravidanza con sindrome dell'ovaio policistico (PCOS), hanno valutato se il suo uso potesse ridurne le complicanze (J Endocrinol Invest. 2013 Nov;36 (10):797-802).
Gli Autori hanno cercato di recuperare le prove rilevanti e le recensioni e liste di riferimento degli articoli selezionati. L'esito primario era l'incidenza delle complicanze della gravidanza, che comprendevano l’EPL (early pregnancy loss), il GDM (gestational diabetes mellitus), la PE (pre-eclampsia) e il PD (preterm delivery).
In totale, erano inclusi otto studi con 1.106 pazienti. I pool degli odds ratio (OR) di risultato con intervallo di confidenza 95% per le donne incinte con PCOS e prescrizione di metformina erano 0,32 (0,19-0,55) per l’EPL, 0.37 (,25-,56) per il GDM, 0.53 (,30-0,95) per il PE e 0,30 (0,13-0,68) per il PD.
In conclusione, la terapia durante la gravidanza con metformina diminuiva l'OR dell’EPL, del GDM, del PE e del PD nelle donne in gravidanza affette da PCOS con gravi effetti dannosi collaterali.
Dal loro canto, Bertoldo MJ dell’Institut National de la Recherche Agronomique, Centre Val de Loire, France e collaboratori, considerando l’azione sensibilizzatrice della metformina sull’insulina, peraltro ampiamente utilizzata nel trattamento della sindrome dell'ovaio policistico (PCOS) e del diabete gestazionale, hanno prodotto una revisione con l’intento di fornire una sintesi sulla sicurezza del farmaco nei vari aspetti della riproduzione sessuale nelle madri gravide e sui possibili effetti collaterali sulla loro prole (Ann Transl Med. 2014 Jun;2 (6):55).
Questo farmaco, in effetti, aveva dimostrato di attivare la protein chinasi 5’AMPK o AMPK, presente in molti tessuti che risentivano, pertanto, del suo effetto. Pur tuttavia, poiché la metformina attraversa la placenta, il suo uso durante la gravidanza suscitava preoccupazioni per quanto riguardava i potenziali effetti negativi sulla madre e sul feto. In effetti, la maggior parte delle segnalazioni suggeriva effetti negativi significativi o teratogenicità. Peraltro, sconcertanti notizie di una riduzione delle dimensioni dei testicoli, del formato dei tubuli seminiferi e del numero delle cellule del Sertoli sui topini maschi esposti in utero al farmaco suggerivano la presenza di suoi effetti non completamente noti.
Jie Sun della Southeast University, Nanjing, People’s Republic of China e collaboratori hanno voluto studiare gli effetti terapeutici della metformina con le statine nella sindrome dell'ovaio policistico (BMJ Open
2015;5: e007280).
Gli Autori hanno, così, svolto una ricerca bibliografica fino all’Ottobre 2014, analizzando i dati di quattro studi di statine e metformina a confronto con la sola metformina.
La combinazione dei due farmaci riduceva i livelli della proteina C reattiva con SMD (standardised mean difference) -0,91; IC 95%= -1,81 a -0,02; p = 0,046), dei trigliceridi con SMD -1,37; IC 95%= -2,46 a -0.28; p = 0,014), del colesterolo totale con SMD -1,28; IC 95%= -1,59 a -0,97; p = 0.000) e delle LDL
(low-density lipoprotein) con SMD -0,74; IC 95%= -1,03 A -0,44; p = 0.000). Tuttavia, la terapia combinata non riusciva a ridurre l’insulina a digiuno (SMD -0,92; IC 95%= -2,07 a 0,24; p = 0.120), il modello di valutazione di omeostasi della resistenza all'insulina (SMD -1,15; IC 95%= -3,36 A 1,06; p = 0,309) e il testosterone totale (SMD -1,12; IC 95%= -2,29 a 0,05; p = 0,061).
L’analisi di cinque trial sulle statine a confronto con il placebo mostrava che la statina in monoterapia riduceva il colesterolo totale, le LDL e i trigliceridi.
In conclusione, le statine combinate alla metformina nelle donne con PCOS potevano migliorare i parametri lipidici e dell’infiammazione, ma non potevano effettivamente migliorare la sensibilità all'insulina e ridurre l’iperandrogenismo.
Negar Naderpoor della Monash University, Melbourne - Australia e collaboratori hanno condotto una revisione sistematica ed una meta-analisi per confrontare l'effetto dello stile di vita in aggiunta alla metformina con quello in aggiunta al placebo e quello della metformina da sola con lo stile di vita con il placebo nella PCOS (Hum. Reprod. Update (2015) doi: 10.1093/humupd/dmv025).
Gli Autori hanno, così, compiuto una ricerca bibliografica fino all’agosto 2014, identificando 2.372 studi e selezionandone dodici per l'analisi. Erano comprese 608 donne con PCOS. Lo stile di vita + metformina (1.5 - 2 g/die) si associavano con una BMI inferiore (differenza media (MD) -0,73 kg / m2, gli intervalli di confidenza (IC) al 95% -1,14, -0,32, p = 0,0005) e con minore tessuto adiposo sottocutaneo (MD -92,49 cm2, IC 95% -164,14, -20,84; p = 0.01). Correlavano anche con un aumento del numero di cicli mestruali (MD 1,06, IC 95% 0.30, 1.82, p = 0.006) dopo sei mesi rispetto allo stile di vita ± placebo. Non vi erano differenze in altri esiti antropometrici, metabolici (indicatori d’insulino-resistenza, di glucosio, di lipidi e della pressione del sangue), della sfera riproduttiva (iperandrogenismo clinico e biochimico) e psicologici (qualità della vita) dopo 6 mesi tra lo stile di vita + metformina confrontati con lo stile di vita ± placebo. Con la sola metformina, rispetto al placebo ± lo stile di vita, il peso e l’indice di massa corporea erano simili dopo 6 mesi, ma il testosterone era inferiore con la metformina.
In conclusione, nell'arco di 6 mesi lo stile di vita + metformina si associava con minore tessuto adiposo sottocutaneo e BMI e migliorava le mestruazioni nelle donne con PCOS rispetto allo stile di vita ± il placebo. La sola metformina confrontata con lo stile di vita dimostrava una simile BMI a 6 mesi. Questi risultati suggerivano che la combinazione dello stile di vita con la metformina avesse un ruolo nella gestione del peso, una delle principali preoccupazioni per le donne con PCOS. Le limitazioni dello studio includevano la campionatura di piccole dimensioni, la breve durata e il rischio di bias.
Metformina, diabete mellito, NAFLD (Non-alcoholic fatty liver disease) e NASH (Nonalcoholic Steatohepatitis)
La NAFLD (nonalcoholic fatty liver disease), in genere a decorso clinico benigno, è la forma più comune di epatopatia. La sua prevalenza nella popolazione generale varia dal 5 al 33%. Da qualche tempo, essa è ormai considerata non un banale accumulo di lipidi nel fegato, ma una patologia con netti rapporti con varie altre malattie, tra cui il diabete. La sua storia naturale si sviluppa attraverso quattro stadi: la steatosi (o fegato semplice grasso), la steatoepatite non alcolica (NASH), la fibrosi e la cirrosi.
La sua forma progressiva, la steatoepatite non alcolica (NASH), è, per suo conto, una condizione potenzialmente grave con conseguente progressione nel 25% dei casi verso la cirrosi, comprese le complicanze a lungo termine dell’ipertensione portale, dell’insufficienza epatica e del carcinoma epatocellulare. Quest'ultima evenienza, peraltro, può verificarsi anche in NASH senza evidenza di cirrosi.
Nella PCOS l’IR sembra giocare un ruolo chiave per lo sviluppo della NAFLD e il diabete ed è stato descritto come un fattore di rischio per la progressione della SH (simple hepatic steatosis) verso la fibrosi. La biopsia epatica, pur tuttavia, anche se ancora serve come gold standard per la distinzione tra SH e NASH, può individuare diverse complicanze dovute al suo carattere invasivo. In via alternativa, per valutare la NASH può servire, come metodo non invasivo, la morte cellulare per apoptosi.

In effetti, l’apoptosi degli epatociti svolge un ruolo importante nella progressione del danno epatico verso la NASH e le altre varie malattie del fegato. Difatti, la morte cellulare per apoptosi degli epatociti è tipicamente migliorata nella NASH, ma è assente nella SH.
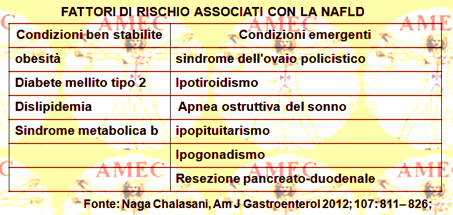
La PCOS, in effetti, è fortemente associata con la NAFLD, diagnosticata dall’elevazione dell’aspartato aminotransferasi (AST) e / o dall’ecografia.
Siccome l’IR svolge un ruolo chiave nella fisiopatologia della PCOS, gli agenti insulinsensibilizzanti sono ampiamente studiati e utilizzati nel trattamento della sindrome dell'ovaio policistico. Questo è, soprattutto, il caso della metformina (MF), agente farmacologico più comunemente usato. Come agente sensibilizzante all’insulina con conseguente riduzione della secrezione epatica di glucosio e aumento del suo utilizzo periferico con effetti positivi sull’IR, sul peso corporeo e sul ciclismo mestruale, nella PCOS il farmaco può influenzare positivamente lo sviluppo della NASH. Per esempio, risulterebbe favorevole la soppressione dell'attività carbossilasi acetil-CoA e dell'accumulo di adenosina monofosfato negli epatociti con conseguente inibizione dell’ossidazione mitocondriale degli acidi grassi e il blocco del glucagone negli epatociti. Già alcuni studi hanno riportato un effetto benefico della MF sulla funzione del fegato e dei suoi enzimi.
La PCOS è un endocrinopatia frequente e include un'alta percentuale di giovani donne, che sono potenzialmente ad alto rischio di grave malattia epatica. L’IR, come detto, svolge un ruolo chiave nella fisiopatologia di entrambe le entità, PCOS e NAFLD. Gli studiosi ipotizzano che una terapia di sei mesi con MF possa influenzare positivamente l’assetto sierologico che definisce la NASH, migliorando l’IR delle pazienti con PCOS.
Al congresso annuale dell’aprile 2015 a Vienna l’EASL (European Association for the Study of the Liver), nel festeggiare anche i suoi primi cinquanta anni di attività, ha colto l’occasione di ribadire lo stretto legame che unisce la diabetologia con l’epatologia.
Difatti, è stato presentato uno studio che dimostrava come la remogliflozina etabonato, farmaco sperimentale antidiabetico, possa costituire una possibile opzione per il trattamento della NASH e della NAFLD.
Lo studio comprendeva 336 diabetici di tipo 2 con emoglobina glicata tra il 7 e 9,5%, randomizzati a diversi dosaggi di remogliflozina (50, 100, 250 o 1000 mg due volte il dì) contro placebo, o pioglitazone (30 mg/die).
La remogliflozina dopo dodici settimane migliorava del 6-33% la sensibilità insulinica e del 23-34% la funzione delle beta cellule. Nei pazienti trattati, inoltre, si otteneva un significativo calo ponderale di 1,4-3,6 Kg, rispetto al gruppo placebo. L’analisi alla dodicesima settimana post-hoc sulla variazione dei livelli delle transaminasi evidenziava anche riduzioni significative nei soggetti trattati con remogliflozina dal 32 al 42%, rispetto al gruppo placebo.
La remogliflozina dimostrava, in effetti, un miglioramento notevole della sensibilità all’insulina e della funzione delle cellule beta pancreatiche, portando anche alla riduzione del peso corporeo e dei livelli delle transaminasi (ALT). Inoltre, studi preclinici hanno fornito prove che riduceva in maniera significativa l’accumulo dei grassi nel fegato, producendo una marcata riduzione dei livelli circolanti dei marcatori dello stress ossidativo. Documentava, in effetti, un’attività anti-ossidante intrinseca, misurata dal test ORAC (oxygen radical antioxidant capacity), capace di correggere la steatoepatite e lo stress ossidativo associato con la NASH. Tutto ciò risultava a differenza degli altri farmaci della stessa classe (SGLT-2 inibitori).
Markus Peck, segretario generale dell’European Association for the Study of the Liver, ha ribadito come la NAFLD e la NASH fossero entrambe fortemente associate al diabete e all’obesità. Queste malattie, difatti, rappresentano nei Paesi economicamente evoluti la principale causa di epatopatia.
Peraltro, la NAFLD doveva essere ormai considerata molto più che un fegato grasso. Questa patologia suole associarsi, infatti, a un rischio aumentato del 50% delle malattie cardiovascolari. Un vasto studio di coorte britannico su circa un milione di persone l’aveva dimostrato chiaramente, evidenziando nelle forme più gravi una probabilità di decesso superiore del 50%, rispetto al resto della popolazione.
Peraltro, è ben noto come i tassi dell’obesità nel mondo siano in continua crescita, in specie nei Paesi più sviluppati, e come nel corso degli ultimi venti anni sia stato ben documentato l'aumento medio della BMI durante la gravidanza.
Tale ultimo dato si è associato anche a un sostanziale aumento medio del peso alla nascita, destando, invero, preoccupazione per le accresciute probabilità dell’obesità infantile e adulta, come dimostrato dagli studi di revisione sistematica. È stato anche segnalato che i bambini, grandi alla nascita per l'età gestazionale con madri obese nella vita intrauterina, dimostravano da adulti un aumentato rischio della sindrome metabolica e della morte prematura. Ne è conseguito che l'aumento dei tassi di obesità materna rappresenta l’avvio di un circolo vizioso con aumento del peso alla nascita e del tasso di obesità infantile e adulta. Tale dato contribuirebbe, invero, all'epidemia dell'obesità cui stiamo assistendo e che è diventata ormai uno dei fattori più significativi per la compromissione della salute globale.
Zobair Younossi dell’Inova Health System in Falls Church, Virginia e collaboratori, per verificare come la steatosi epatica non alcolica stesse emergendo come una delle principali cause del carcinoma epatocellulare, dal 2004 al 2009 hanno identificato 5.748 pazienti con carcinoma epatocellulare e 17.244 soggetti di controllo senza cancro (Expert Rev Endocrinol Metab. 2013;8 (6):549-558. © 2013).
Gli Autori, in effetti, dimostravano come nel periodo studiato l'aumento annuale del carcinoma epatocellulare nei pazienti con malattia del fegato grasso fosse stato di circa il 5%. Peraltro, la sopravvivenza in questi pazienti era più breve, rispetto a quelli con l’epatite B o C che sviluppavano la neoplasia. Al momento della diagnosi, era più avanzato anche lo stadio del tumore e il trapianto di fegato era meno comune. Dato più preoccupante era che l'epidemia del fegato grasso non alcolico e il peso delle complicanze correlate alla malattia erano destinati a crescere.
Gli Autori affermavano che la steatosi epatica colpiva, di fatto, circa il 25% della popolazione degli Stati Uniti, configurandosi in circa il 2% e il 3% nella forma progressiva di steatoepatite non alcolica.
Questa forma patologica, maggiormente a rischio di esiti negativi, poteva essere stabilita con sicurezza con la biopsia epatica, pratica invasiva eseguita nella piccola minoranza dei pazienti. Pertanto, un gran numero di diagnosi non veniva portata a termine senza il riconoscimento anche di una fibrosi avanzata a rischio di carcinoma epatocellulare.
La loro raccomandazione era, quindi, di determinare se un paziente con fegato grasso avesse la steatoepatite con fibrosi avanzata o cirrosi. Era raccomandata, pertanto, la necessità di screening ogni sei mesi per il carcinoma epatocellulare.
Dal 2004 al 2009, il dottor Younossi e colleghi identificavano dai database -Medicare SEER (Surveillance, Epidemiology, and End Results) 5.748 pazienti con carcinoma epatocellulare e 17.244 soggetti di controllo senza cancro.
Si rilevava, così, che il cancro del fegato era legato nel 48% dei casi all’epatite C, nel 26% al fegato grasso, nel 14% alla malattia epatica alcolica, nell’8% all’epatite B e nel 4% all’epatite autoimmune o alla cirrosi biliare.
Susanne Tan dell’University of Duisburg-Essen, Germany e collaboratori hanno, per loro conto, voluto valutare l'influenza della metformina sulla NASH in pazienti con PCOS (Int J Endocrinol. 2015; 2015: 254169).
Gli Autori poggiavano il loro studio sulla base che la sindrome dell'ovaio policistico (PCOS), com’era noto, era associata all’obesità e all’insulino-resistenza (IR), caratteristiche chiave della steatoepatite non alcolica (NASH). I frammenti della proteina Cytokeratin 18 (M30) erano stabiliti come marcatori sierici per la NASH e la metformina come sensibilizzante dell’insulina per il miglioramento dell’IR epatica.
Si valutavano in ottantanove pazienti i parametri metabolici, il danno epatico indicando al basale e dopo il trattamento con metformina il LIFL (liver injury indicating fatty liver) e il M30. Le pazienti con iniziale IR erano suddivise in IR risolta (PCOS-Exir) e in persistente (PCOS-PIR) dopo il trattamento, rispetto a un gruppo di PCOS inizialmente sensibili all'insulina (PCOS-C). La prevalenza del miglioramento della LIFL si sarebbe potuta vedere nelle PCOS-C e nelle PCOS-Exir, rispetto alle PCOS-PIR (-19,4, risp., -12,0% rispetto al 7,2%, Chi (2) = 29.5, p <0,001), senza variazione di quella della NASH. Nelle PCOS-PIR i livelli delle ALT aumentavano significativamente, accompagnati da un aumento nominale non significativo della M30.
In conclusione, la metformina migliorava il LIFL nei sottogruppi di pazienti con PCOS, senza influenzare la NASH. Tutto ciò, secondo gli Autori, avrebbe potuto significare un effetto mancante della metformina sulla NAFLD o sul rallentamento della progressione della malattia.
Dal loro canto, S. Gitto dell’Università di Modena e Reggio Emilia, Italy e collaboratori hanno analizzato nella loro recensione bibliografica il rapporto tra gli aspetti molecolari complessi della NASH e le opzioni terapeutiche più interessanti e promettenti a riguardo (Gastroenterology Research and PracticeVolume 2015 (2015), Article ID 732870, 14 pages).
Gli Autori precisavano che la definizione della NAFLD (steatosi epatica non alcolica) doveva essere rappresentata da una steatosi oltre il 5-10% del peso totale dell’organo. Per una diagnosi accurata bisognava escludere con tecniche d’immagini o istologiche le altre cause di accumulo del grasso, come il consumo eccessivo di alcol (donne ≤20 g / d, uomini ≤30 g / d). Inoltre, si sarebbero dovute esplorare altre cause di steatosi macrovescicolare secondarie, come la nutrizione parenterale, l'epatite C, il morbo di Wilson, gli stati di fame, la lipodistrofia, l’abetalipoproteinemia e i farmaci (ad esempio il metotrexate, l’amiodarone e gli steroidi). Peraltro, i medici avrebbero dovuto cercare altre origini di steatosi micro vescicolare, come la sindrome di Reye, il fegato grasso acuto in gravidanza, la sindrome di HELLP (Hemolysis - Elevated Liver enzymes - Low Platelet count), i disturbi metabolici (ad esempio carenza di lecitina-colesterolo-aciltransferasi) e l'uso di farmaci (ad esempio, gli antiretrovirali o il valproato).
Nei riguardi della metformina, gli Autori affermavano che era ben noto che potesse influenzare positivamente l’insulinoresistenza, uno dei pilastri della patogenesi della NASH. Di conseguenza, era ampiamente studiato il possibile ruolo di questo farmaco nel trattamento della malattia epatica metabolica.
Nel 2004 Nair e collaboratori avevano pubblicato un piccolo studio in aperto riferendo che una terapia di tre mesi con metformina era stata in grado di diminuire solo transitoriamente i livelli delle ALT / AST. Sorprendentemente, gli Autori avevano riportato una mancanza di miglioramento significativo sia dell’infiammazione epatica e sia della fibrosi. In un piccolo studio pilota, Loomba e collaboratori avevano dimostrato che quarantotto settimane di metformina (2.000 mg / die) non avevano avuto alcun effetto significativo sulle caratteristiche istologiche della NASH. L'anno seguente, Haukeland e collaboratori avevano sviluppato uno studio più significativo. Gli Autori avevano arruolato quarantotto pazienti con NAFLD dopo biopsia in un RCT con metformina o placebo per sei mesi. Era stata confermata l'assenza di alterazioni istologiche come risultato del farmaco, ma era stata osservata una diminuzione dei livelli sierici di entrambi i lipidi e del glucosio.
Inoltre, in un RCT con metformina (500-1000 mg il giorno per dodici mesi) contro placebo, Shields e collaboratori confermavano l'assenza di un significativo effetto positivo sull’istologia epatica e anche la mancanza di una significativa perdita di peso.
Una revisione sistematica di otto RCT non aveva dimostrato effetti favorevoli della metformina sull’istologia NASH, anche se aveva potuto portare alla perdita di peso. Infatti, anche se la metformina poteva essere utilizzata in pazienti diabetici con NASH, non esisteva alcuna prova a sostegno della sua efficacia nei termini dell’istologia della malattia.
Metformina (glucophage) e irsutismo
Il termine d’irsutismo nella donna indica la crescita eccessiva dei capelli con una loro distribuzione di tipo maschile. Questa penosa condizione per le pazienti presenta, invero, anche una sfida di gestione clinica. In circa il 90% delle donne con irsutismo la malattia di base è la PCOS (polycystic ovary syndrome) nella sua forma intrinseca d’iperandrogenismo o di quell’idiopatica correlata a un aumento della sensibilità dei tessuti agli androgeni. In effetti, un’elevata percentuale delle pazienti con irsutismo idiopatico dimostra ovaie policistiche, il che suggerisce che queste due forme non possono essere facilmente distinguibili. La PCOS, come in precedenza riportato, è una malattia eterogenea caratterizzata da anovulazione cronica, iperandrogenismo e iperinsulinemia secondaria alla ridotta sensibilità all'insulina. La maggiore secrezione degli androgeni ovarici è considerata determinata dall’aumentata secrezione degli steroidi da parte delle cellule ovariche per stimolazione dell’insulina stessa, ma anche dai fattori di crescita insulinosimili, tra cui l’IGF-I, e da una diminuzione dell’attività dell’IGFBP (IGF-binding protein). L’iperandrogenismo si manifesta comunemente nel 60-83% dei casi con l’irsutismo, nell’11-43% con l’acne, la seborrea e l’alopecia. Gli androgeni hanno dimostrato di essere responsabili, almeno parzialmente, della promozione della fase anagen (fase di crescita) del ciclo del capello con aumento di dimensione dei follicoli e il cambiamento da vellus allo stato pilifero terminale. Studi in vitro hanno, peraltro, dimostrato che l’androgeno, attivo in tal senso, è il 5 α -dihydrotestosterone, prodotto localmente dall'azione dell’enzima 5 α reduttasi sul testosterone. Si è anche dimostrato che la fase anagen è influenzata dal fattore di crescita IGF-I, trasportato in circolo prevalentemente dagli IGFBP specifici, ma anche prodotto localmente dalla papilla dermica. In tale sede agisce sia sul derma e sia sull'epidermide. L'attività di tutti questi fattori di crescita dipende da una serie di fattori, sia locali e sia circolanti, relativi alle proteine di legame, a loro volta anche influenzati dalle azioni dell’insulina. Così che, le donne con PCOS possono manifestare anomalie nel metabolismo di entrambi i principali fattori responsabili dell’irsutismo: gli androgeni da una parte e l’insulina e i fattori di crescita dall’altra.
Le donne con PCOS soffrono di un'alta incidenza di acne, anch’essa collegata con le concentrazioni in circolo degli androgeni sierici, dell’insulina e dell’IGF-I.
L'uso dei farmaci OAM (oral antihyperglycemic medication), e prevalentemente quello della metformina e dei tiazolidenedioni, hanno dimostrato di migliorare la sensibilità all'insulina e la funzione ovarica. In particolare, in un certo numero di studi il trattamento con metformina ha permesso di rilevare una riduzione dei livelli circolanti dell’insulina, dello LH, dell’androstenedione e delle concentrazioni del testosterone. Il trattamento di lunga durata ha portato anche a miglioramenti dell'indice di massa corporea (BMI), alla regolazione del ciclo mestruale, a tassi di ovulazione naturale e di gravidanza spontanea e assistita. Si è ipotizzato che, riducendo le concentrazioni circolanti d’insulina e di conseguenza quelle degli androgeni liberi, le OAM sarebbero in grado di migliorare l’irsutismo.
Christopher J G Kelly e Derek Gordon della North Glasgow University NHS, UK hanno voluto valutare in uno studio in doppio cieco cross-over, controllato con placebo, l'effetto della metformina sulla crescita dei capelli (European Journal of Endocrinology 147 217–221).
Gli Autori hanno, quindi, arruolato sedici donne con PCOS e irsutismo in quattordici mesi (due fasi di sei mesi con due di washout).
Hanno valutato l’irsutismo utilizzando il punteggio della velocità di crescita F-G (Ferriman and Gallwey) e quello di autovalutazione della paziente. Si registravano: peso, altezza, rapporto vita-fianchi, gonadotropine, androgeni, glicemia e lipidi.
Dieci donne completavano lo studio dei quattordici mesi con un significativo miglioramento dell’irsutismo al termine della fase della metformina rispetto a quella del placebo. Il punteggio FG era 15.8 + 1,4 per la metformina contro 17.5 + 1.2 del placebo (P= 0.025). L’autovalutazione delle pazienti era 2.4 + 0.1 vs 3.3 + 0.3 (P = 0.014). Migliorava anche la velocità di crescita in millimetri il giorno al termine di ogni fase (0.67 + 0.17 vs 0.77 + 0.11; P= 0.03)
Non c'era un significativo miglioramento sia della SHBG (sex hormone binding globulin) e del FAI (free androgen index), anche se c'era una differenza importante tra il basale e il trattamento con metformina per lo SHBG (P = 0.023) e per il FAI (P= 0.036). Il trattamento con metformina riduceva significativamente anche il peso (91,5 + 7,6 vs 94,0 + 9,8 kg; P = 0.009) e portava a un miglioramento significativo della frequenza del ciclo (0.53 + 0.12 vs 0.35 + 0.08 cicli il mese; P = 0.008).
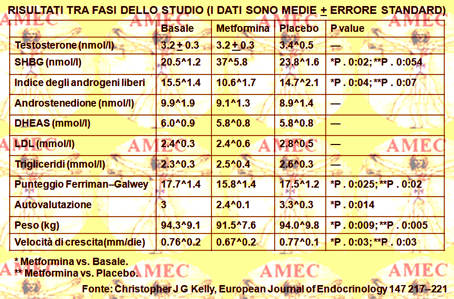
In conclusione, gli Autori ritenevano di aver dimostrato che il trattamento con metformina in un gruppo di donne con PCOS risultava, rispetto al placebo, in un miglioramento clinicamente e statisticamente significativo nella crescita dei capelli.
Dal loro canto, Lyndal Harborne della Royal Infirmary, Glasgow, Scotland, United Kingdom e collaboratori hanno voluto confrontare in uno studio, in cui l’irsutismo rappresentava l'end point primario, l'efficacia della metformina con quella di un trattamento combinato di etinilestradiolo e ciproterone acetato (J Clin Endocrinol Metab 88: 4116–4123, 2003).
Gli Autori randomizzavano, così, per 12 mesi 52 pazienti a metformina (500 mg, tre volte il giorno) o Diane (etinilestradiolo 35 µg più ciproterone acetato 2 mg) con valutazioni prima del trattamento, a sei e a dodici mesi. Si utilizzavano entrambi i metodi oggettivi e soggettivi di valutazione dell’irsutismo e, in aggiunta, si esaminavano le percezioni della paziente.
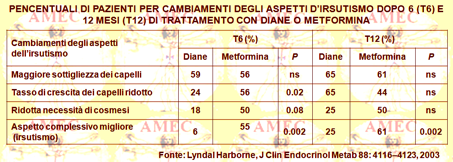
I risultati mostravano che la metformina era potenzialmente efficace nelle donne con PCOS con irsutismo da moderato a grave. Inoltre, suggerivano che in alcuni aspetti il punteggio Ferriman-Gallwey e dell’autovalutazione della paziente era maggiore di quello del trattamento standard con Diane. La valutazione obiettiva della riduzione del diametro dei capelli in più sedi anatomiche dimostrava che entrambi i trattamenti erano moderatamente efficaci. D’altra parte, il trattamento con Diane era responsabile di una profonda soppressione dell'attività androgenica, in contrasto con la metformina che induceva un cambiamento solo trascurabile. Tuttavia, riducendo la metformina i marcatori dell’insulino-resistenza, si evinceva che l’irsutismo poteva essere trattato efficacemente moderando l’iperinsulinemia.
Ester J. van Zuuren della Leiden University Medical Center, Netherlands e collaboratori dal Cochrane Skin Group hanno voluto valutare gli effetti degli interventi per l’irsutismo, fatta eccezione per il laser e le terapie a base di sola luce, (Cochrane Database Syst Rev. 2015 Apr 28;4: CD010334).
Gli Autori commentavano che l’irsutismo si verificava nel 5-10% delle donne in età riproduttiva, rappresentando un disturbo fastidioso con un notevole impatto sulla qualità della vita perché fonte di stress psicologico, bassa autostima e disagio sociale. La causa più comune era, in effetti, la sindrome dell'ovaio policistico con molte opzioni di trattamento, ma senza chiare loro indicazioni di efficacia.
Procedevano, così, a una ricerca in letteratura scientifica fino al giugno del 2014, selezionando studi clinici randomizzati e controllati (RCT) nelle donne irsute con sindrome dell'ovaio policistico, irsutismo o iperandrogenismo idiopatico.
S’includevano 157 studi con dimensione del campione da trenta a ottanta, comprendenti 10.550 donne di età media di venticinque anni. Il rischio di bias era alto in 123 studi, poco chiaro in trenta e basso in quattro. La mancanza di attenzione era la fonte più frequente dei bias. La durata del trattamento variava da sei a dodici mesi. Quarantotto studi fornivano dati non utilizzabili o recuperabili, vale a dire per mancanza dei dati separati per le donne irsute, degli atti dei convegni e per le perdite dei follow-up sopra il 40%. Gli esiti primari, come il miglioramento dell’irsutismo riportato dalle partecipanti e il cambiamento correlato alla salute e alla qualità della vita, erano affrontati in pochi studi. Gli eventi avversi lo erano solo per la metà. Nella maggior parte dei confronti non c'erano prove sufficienti per determinare se vi fosse differenza nel numero degli eventi avversi riportati. Essi, peraltro, includevano i disturbi gastrointestinali, la tensione mammaria, la riduzione della libido, la pelle secca per la flutamide e la finasteride. Per lo spironolattone comprendevano il sanguinamento irregolare, per la metformina la nausea la diarrea e il gonfiore dell’addome, per gli analoghi del GnRH (gonadotropina-releasing hormone) le vampate di calore, la secchezza vaginale e il mal di testa. La valutazione del medico dell’irsutismo e la variazione dei livelli degli androgeni erano affrontate nella maggior parte dei confronti, mentre le variazioni dell'indice di massa corporea (BMI) e il miglioramento degli altri segni clinici dell’iperandrogenismo solo in un terzo degli studi. La qualità dell'evidenza variava da moderata a molto bassa per la maggior parte degli esiti. Vi era evidenza di bassa qualità per l'effetto di due OCP (oral contraceptive pill) (etinilestradiolo + ciproterone acetato rispetto all’etinilestradiolo + desogestrel), rispetto al basale, sul cambiamento dei punteggi Ferriman-Gallwey. La differenza media (MD) era -1,84 (intervallo di confidenza (IC)95%= -3,86 a 0,18). Vi era prova molto bassa di qualità che la flutamide 250 mg due volte il giorno riducesse, in modo più efficace rispetto al placebo, i punteggi di Ferriman-Gallwey (-7,60 MD, IC 95%= -10,53 a -4,67 e -7,20 MD, IC 95%= -10,15 a -4.25). In uno studio le valutazioni delle venti partecipanti confermavano una risk ratio (RR) di 17.00 e un IC 95%= 1,11-259,87. Lo spironolattone 100 mg il giorno era più efficace del placebo con prove di bassa qualità nel ridurre i punteggi di Ferriman-Gallwey (MD -7,69, l’IC 95%= -10,12 a -5,26). Si dimostrava, in due studi con prove di molto bassa qualità, un’efficacia simile alla flutamide (MD -1.90, IC 95%= -5,01 a 1,21 e 0,49 MD, IC 95%= -1,99 a 2,97), così come alla finasteride con prove di bassa qualità in due studi (MD 1,49, IC 95%= -0,58 a 3,56 e 0,40 MD, IC 95% -1,18 a 1,98). Anche se non vi erano prove di qualità molto bassa di una differenza nella riduzione dei punteggi di Ferriman-Gallwey per la finasteride da 5 a 7,5 mg il giorno rispetto al placebo (-5,73 MD, IC 95%= -6,87 a -4,58), era improbabile che ciò fosse clinicamente significativo. Questi risultati erano rafforzati dalle valutazioni delle partecipanti (RR 2,06, IC 95%= 0,99-4,29 e RR 11,00, IC 95%= ,69-175,86). Tuttavia, la finasteride mostrava risultati coerenti in confronto con altri trattamenti senza, però, potersi raggiungere alcuna conclusione definitiva. La metformina nella riduzione dei punteggi di Ferriman-Gallwey non dimostrava alcun beneficio rispetto al placebo (MD 0,05, IC 95%= -1,02 a 1,12), ma la qualità delle prove era bassa. I risultati sull'efficacia degli analoghi dello GnRH erano inconsistenti e variavano da un minimo miglioramento a uno importante. Non si era in grado di riunire i dati del lotto per l’OCP con ciproterone acetato da venti a 100 mg a causa dell’eterogeneità clinica e metodologica tra gli studi. Tuttavia, l'aggiunta del ciproterone acetato all’OCP forniva una maggiore riduzione nei punteggi di Ferriman-Gallwey. Due studi, che avevano confrontato la finasteride 5 mg e lo spironolattone 100, non mostravano con prove di bassa qualità differenze nelle valutazioni delle partecipanti e nella riduzione dei punteggi di Ferriman-Gallwey. I punteggi di Ferriman-Gallwey, provenienti da tre studi di confronto tra la flutamide rispetto alla metformina, non potevano essere messi insieme (I² = 62%). Uno studio, che confrontava la flutamide 250 mg due volte il giorno con la metformina 850 mg due volte il giorno per dodici mesi e che raggiungeva un più alto dosaggio cumulativo di altri due studi che avevano valutato questo confronto, dimostrava con prova di qualità molto bassa che la flutamide era più efficace (MD -6,30, IC 95%= -9,83 a - 2.77). Le riduzioni in quattro studi di confronto tra la finasteride con la flutamide che mostravano i dati nei punteggi di Ferriman-Gallwey non potevano essere messe insieme, poiché i risultati erano inconsistenti (I² = 67%). Gli studi sugli effetti delle diete ipocaloriche segnalavano la riduzione della BMI, ma non dei punteggi di Ferriman - Gallwey. Non s’individuavano RCT rilevanti su alcune misure cosmetiche, anche se comunemente usate.
In conclusione, i trattamenti potevano avere bisogno di comprendere terapie farmacologiche, procedure di cosmetici e supporto psicologico. Per l’irsutismo mite vi erano prove di qualità limitata che le OCP potessero essere efficaci. La flutamide 250 mg due volte il giorno e lo spironolattone 100 mg il giorno sembravano essere efficaci e sicuri, anche se con prova di qualità da bassa a molto bassa. La finasteride 5 mg il giorno aveva dimostrato risultati incoerenti in diverse comparazioni senza poter offrire, quindi, alcuna conclusione definitiva. Poiché gli effetti collaterali degli antiandrogeni e della finasteride erano ben noti, bisognava contabilizzarli in qualsiasi processo decisionale clinico. C'erano prove di bassa qualità che la metformina potesse essere inefficace per l’irsutismo e, anche se gli analoghi dello GnRH avevano dimostrato risultati inconsistenti nella sua riduzione, essi riscuotevano un notevole effetto sulla ricerca.
Metformina (glucophage) e TSH (thyroid-stimulating hormone)
Alcuni studi, nonostante l’eccellente profilo di sicurezza della metformina, hanno evidenziato che il suo uso può abbassare i livelli del TSH (thyroid-stimulating hormone) nei pazienti con diabete e con ipotiroidismo. Tale dato portava a considerare una potenziale esposizione a conseguenze dannose d’ipertiroidismo subclinico, come condizioni cardiovascolari e fratture. Bisogna precisare che tale condizione non si è riscontrata nelle persone sane eutiroidee.
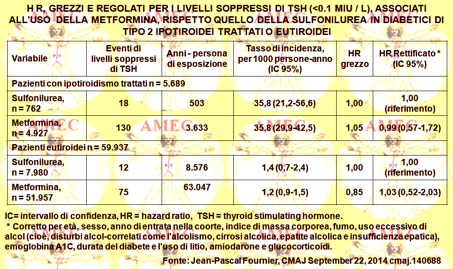
Jean-Pascal Fournier della McGill University, Montréal, Quebec e collaboratori hanno inteso determinare se nei pazienti con diabete di tipo 2 l'uso della metformina in monoterapia, rispetto a quella con sulfonilurea, si associasse a un aumentato rischio di basso TSH (<0.4 mIU / L) in ipotiroidei ed eutiroidei (CMAJ September 22, 2014 cmaj.140688).
Gli Autori facevano notare che la base d’incertezza sull'uso della metformina nei diabetici di tipo 2 con ipotiroidismo o eutiroidismo era determinata dalle carenze metodologiche e dalla scarsità degli studi condotti.
Utilizzando il Clinical Practice Research Datalink, si identificavano i pazienti con inizio di terapia con metformina o con sulfonilurea in monoterapia tra il primo gennaio 1988 e il 31 dicembre 2012. Si formavano due gruppi di pazienti di almeno quaranta anni di età con ipotiroidismo o eutiroidismo, trattati e seguiti fino al 31 marzo 2013. Si utilizzavano modelli proporzionali di Cox per valutare in ogni sottocoorte l'associazione tra i bassi livelli del TSH con metformina in monoterapia, rispetto alla monoterapia con sulfonilurea.
Si arruolavano 5.689 pazienti trattati anche per ipotiroidismo e 59.937 eutiroidei. Durante il follow-up si osservavano tra i primi 495 eventi di bassi livelli del TSH (tasso d’incidenza 119,7 / 1000 anni-persona). Nel secondo gruppo si rilevavano 322 eventi di bassi livelli di TSH (tasso d’incidenza 4.5 / 1000 anni-persona). Rispetto alla monoterapia con la sulfonilurea, la metformina in monoterapia si associava a un aumento del rischio del 55% dei livelli di TSH basso nei pazienti con ipotiroidismo (tasso d’incidenza 79,5 / 1000 anni-persona v.125.2 / 1000 anni-persona, hazard ratio aggiustato [HR] 1.55, IC 95%= 1,09-2,20), con il più alto rischio nei 90-180 giorni dopo l'inizio (HR aggiustato 2,30, IC 95%= 1,00-5,29). Nessuna associazione si osservava, invece, nei pazienti eutiroidei (HR aggiustato 0,97; IC 95%= 0,69-1,36).
In conclusione, in questo largo studio longitudinale basato sulla popolazione l'uso della metformina si associava a un aumento dell'incidenza del 55% dei bassi livelli del TSH (sotto gli 0,4 mIU / L) nei pazienti trattati anche per ipotiroidismo, rispetto a quelli trattati con monoterapia di sulfonilurea. Lo stesso non si verificava nei pazienti eutiroidei. I meccanismi biologici esatti che potessero spiegare questa proprietà del farmaco, secondo gli Autori, non erano chiari. Pur tuttavia, poteva trovarsi una spiegazione nell’attivazione dell’adenosina 5'-monofosfato-chinasi attivata (AMPK) in periferia, inibente l’AMPK ipotalamico coinvolto nella regolazione del TSH.
Altri meccanismi proposti comprendevano le modifiche di affinità tiroide-ormone-recettore, tiroide-ormone vincolante, la biodisponibilità e il metabolismo indotti dall’attivazione costitutiva del recettore del TSH e l'interferenza con il dosaggio del TSH.
Metformina, farmaco di longevità nel diabetico
La metformina, invero, in diversi studi clinici e osservazionali ha mostrato sul paziente diabetico tipo 2, rispetto alle sulfaniluree, una diminuzione del rischio di eventi cardiovascolari e di morte.
C. A. Bannister della Cardiff University, UK e collaboratori, non avendo riscontrato in letteratura se ciò potesse essere dovuto agli effetti benefici della metformina o a quelli negativi delle sulfoniluree, hanno voluto confrontare tutte le cause di mortalità nei pazienti diabetici trattati in prima linea con uno dei due farmaci in monoterapia con quelle d’individui abbinati senza la malattia (Diabetes Obes Metab. 2014 Nov;16 (11):1165-73).
Si utilizzavano quindi, i dati osservazionali retrospettivi del CPRD (Clinical Practice Research Datalink) del Regno Unito dal 2000, abbinando con persone senza la malattia, diabetici di tipo 2 che traevano miglioramento dal trattamento di prima linea in monoterapia con metformina o con sulfonilurea. La progressione della mortalità per qualsiasi causa era confrontata con i modelli di sopravvivenza parametrici, comprendenti una serie d’importanti co-variabili.
S’identificavano 78.241 soggetti trattati con metformina, 12.222 con sulfonilurea e 90.463 soggetti appaiati senza diabete. Ciò determinava un periodo di follow-up totale di 503.384 anni. Occorrevano in totale 7.498 morti, pari a tassi non aggiustati di mortalità del 14,4 e del 15,2, del 50,9 e del 28,7 decessi per 1000 persone-anno per la monoterapia con metformina e con sulfonilurea rispettivamente con i loro controlli appaiati. Con riferimento alla sopravvivenza osservata nei pazienti diabetici con metformina in monoterapia [rapporto di tempo di sopravvivenza (STR) = 1.0], il tempo di sopravvivenza rettificato medio era inferiore del 15% (STR = 0,85, IC 95%= 0,81-0,90) nei soggetti abbinati senza diabete e del 38% (0,62, 0,58-0,66) nei trattati con sulfonilurea in monoterapia.
In conclusione, i pazienti con diabete di tipo 2, avviati con metformina in monoterapia, mostravano una sopravvivenza più lunga dei controlli abbinati. Quelli trattati con sulfonilurea manifestavano, peraltro, una sopravvivenza marcatamente ridotta, rispetto sia ai controlli appaiati e sia a quelli trattati con metformina in monoterapia. Questi risultati supportavano la posizione della metformina come farmaco di prima linea nel diabete tipo 2 e implicavano che il farmaco potesse conferire beneficio in una possibile profilassi anche ai non malati della malattia metabolica. Le sulfoniluree rimanevano nel campo di una seria preoccupazione.
Per loro conto, Chen-Pin Wang dell’University of Texas Health Science Center at San Antonio, USA e collaboratori hanno voluto determinare se l'effetto protettivo della metformina contro la mortalità venisse modificato negli anziani con diabete di tipo 2 in base allo stato di fragilità (J Endocrinol Diabetes Obes. 2014;2 (2). pii: 1031).
Gli Autori consideravano che negli Stati Uniti la percentuale della popolazione dell’età dei sessantacinque anni e oltre per il 2030 era prevista in aumento sino al 19,6%, raggiungendo circa i settantuno milioni di individui. Il crescente numero di anziani aumentava, quindi, le responsabilità del sistema sanitario pubblico e dei servizi medici e sociali. Una parte importante delle richieste era legata, peraltro, agli oneri associati al diabete di tipo 2, malattia ormai epidemica e connessa all'invecchiamento. Ne era colpito, in effetti, il 26,9% della popolazione statunitense di sessantacinque anni e oltre. Il diabete di tipo 2 inoltre era indicato come un fattore predittivo importante per la fragilità esacerbata dalla resistenza all'insulina in un circolo vizioso in cui l'azione dell'insulina ridotta contribuiva al processo della malattia e alla conseguente capacità funzionale ridotta che comprometteva ulteriormente l'azione dell'ormone. Ne conseguiva come fatto importante l’identificazione d’interventi pratici che avrebbero potuto ridurre l'onere associato alle malattie legate invecchiamento, come il diabete, e, quindi, promuovere una senilità in salute con longevità. Si ribadiva che la necessità di questo tipo d’interventi era annotata come particolarmente urgente per la popolazione degli Stati Uniti in cui il 44% degli individui aveva un'età uguale o superiore ai sessantacinque anni.
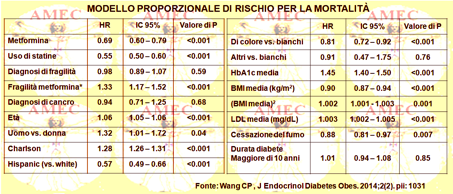
Gli Autori annotavano, in particolare, che alcuni studi avevano in precedenza attribuito l'effetto della metformina sulla riduzione della mortalità principalmente alla sua azione pleiotropica sull’infiammazione e sulla sensibilizzazione all'insulina. Pur tuttavia, questo effetto benefico poteva essere attenuato alla presenza della fragilità, sindrome geriatrica di declino fisico nel tempo con tendenza all’aggravamento. Questo perché questa sindrome può portare a un peggioramento della resistenza all'insulina e della fragilità. La metformina avrebbe potuto contrastare la fragilità inibendo la resistenza all'insulina con netto beneficio sulla mortalità e dei pazienti. In effetti, era ben noto che il diabete con le sue complicanze macrovascolari per effetto della resistenza all'insulina era un predittore significativo dell’insorgenza e della progressione della fragilità.
Gli Autori hanno, così, condotto uno studio di coorte dall’ottobre 1999 al settembre 2006 tra i veterani di età compresa tra i sessantacinque e gli ottantanove anni con diabete di tipo 2, ma senza storia di malattie del fegato, renali o tumori. I partecipanti avevano anche, come unico farmaco antidiabetico per 180 o più giorni, le sulfoniluree o la metformina. Si utilizzava il modello di rischio proporzionale di Cox per confrontare i tassi di rischio della mortalità per qualsiasi causa tra gli utenti dei farmaci, aggiustato per l’indice di propensione d’uso della metformina e delle covariate: età, razza / etnia, durata del diabete, punteggio di comorbidità di Charlson, uso di statine, fumo, BMI, colesterolo LDL e HbA1c.
In questa coorte di 2.415 veterani, 307, il 12,7%, usavano la metformina, 2.108, lo 87,3%, le sulfoniluree. L'età media era di 73,7 ± 5,2 anni, il periodo di studio medio era di 5,6 ± 2,3 anni, la HbA1c media 6,7 ± 1,0%, il 23% aveva il diabete da dieci e più anni e il 43,6%, 1.048 in numeri, decedeva durante il periodo di studio. Per il gruppo dei pazienti con e senza la fragilità della metformina vs quello della sulfonilurea gli hazard ratio aggiustati (HR) di morte erano rispettivamente 0,92 (IC 95% = 0,90-1,31, valore di p = 0,19) e 0,69 (IC 95% = 0,60-0,79, valore di p= <0.001). L’analisi di regressione logistica mostrava che la metformina vs. la sulfonilurea era significativamente associata a una riduzione delle quote di fragilità (OR: 0,66, IC 95%= 0,61-0,71, valore di p= <.0001).
In conclusione, lo studio, secondo gli Autori, suggeriva che la metformina avrebbe potuto potenzialmente promuovere negli anziani con diabete di tipo 2 la longevità attraverso la prevenzione della fragilità.
